Questão ITA 2006 - Soluções
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Questão ITA 2006 - Soluções
Questão ITA 2006 - Soluções
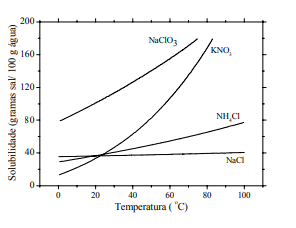
ITA Considere um calorímetro adiabático e isotérmico, em que a temperatura é mantida rigorosamente constante e igual a 40°C. No interior desse calorímetro, é posicionado um frasco de reação cujas paredes permitem a completa e imediata troca de calor. O frasco de reação contém 100 g de água pura a 40ºC. Realizam-se cinco experimentos, adicionando uma massa m1 de um sal X ao frasco de reação. Após o estabelecimento do equilíbrio termodinâmico, adiciona-se ao mesmo frasco uma massa m2 de um sal Y e mede-se a variação de entalpia de dissolução (∆H). Utilizando essas informações e as curvas de solubilidade apresentadas na figura, excluindo quaisquer condições de metaestabilidade, assinale a opção que apresenta a correlação correta entre as condições em que cada experimento foi realizado e o respectivo ∆H.
A) Experimento 1: X = KNO3; m1 = 60 g; Y = KNO3 ; m2 = 60 g; ∆H > 0.
B) Experimento 2: X = NaClO3; m1 = 40 g; Y = NaClO3; m2 = 40 g; ∆H > 0.
C) Experimento 3: X = NaCl ; m1 = 10 g; Y = NaCl; m2 = 10 g; ∆H < 0.
D) Experimento 4: X = KNO3 ; m1 = 60 g; Y = NaClO3; m2 = 60 g; ∆H = 0.
E) Experimento 5: X = KNO3 ; m1 = 60 g; Y = NH4Cl; m2= 60 g; ∆H < 0.
A) Experimento 1: X = KNO3; m1 = 60 g; Y = KNO3 ; m2 = 60 g; ∆H > 0.
B) Experimento 2: X = NaClO3; m1 = 40 g; Y = NaClO3; m2 = 40 g; ∆H > 0.
C) Experimento 3: X = NaCl ; m1 = 10 g; Y = NaCl; m2 = 10 g; ∆H < 0.
D) Experimento 4: X = KNO3 ; m1 = 60 g; Y = NaClO3; m2 = 60 g; ∆H = 0.
E) Experimento 5: X = KNO3 ; m1 = 60 g; Y = NH4Cl; m2= 60 g; ∆H < 0.
- Resposta e minha dúvida:
- R=B
Eu até acertei, mas não entendi o ∆H, de nenhuma alternativa, como ele é calculado?

Mineira_lanes- Padawan

- Mensagens : 52
Data de inscrição : 02/02/2023
Idade : 20
Localização : MG, Brasil
 Re: Questão ITA 2006 - Soluções
Re: Questão ITA 2006 - Soluções
Mineira_lanes, na realidade nao ha necessidade de proceder com nenhum calculo, se no processo de dissolução houve aumento da T significa que ele absorveu calor (∆H > 0), ou seja, processo endotérmico.Mineira_lanes escreveu:ITA Considere um calorímetro adiabático e isotérmico, em que a temperatura é mantida rigorosamente constante e igual a 40°C. No interior desse calorímetro, é posicionado um frasco de reação cujas paredes permitem a completa e imediata troca de calor. O frasco de reação contém 100 g de água pura a 40ºC. Realizam-se cinco experimentos, adicionando uma massa m1 de um sal X ao frasco de reação. Após o estabelecimento do equilíbrio termodinâmico, adiciona-se ao mesmo frasco uma massa m2 de um sal Y e mede-se a variação de entalpia de dissolução (∆H). Utilizando essas informações e as curvas de solubilidade apresentadas na figura, excluindo quaisquer condições de metaestabilidade, assinale a opção que apresenta a correlação correta entre as condições em que cada experimento foi realizado e o respectivo ∆H.
A) Experimento 1: X = KNO3; m1 = 60 g; Y = KNO3 ; m2 = 60 g; ∆H > 0.
B) Experimento 2: X = NaClO3; m1 = 40 g; Y = NaClO3; m2 = 40 g; ∆H > 0.
C) Experimento 3: X = NaCl ; m1 = 10 g; Y = NaCl; m2 = 10 g; ∆H < 0.
D) Experimento 4: X = KNO3 ; m1 = 60 g; Y = NaClO3; m2 = 60 g; ∆H = 0.
E) Experimento 5: X = KNO3 ; m1 = 60 g; Y = NH4Cl; m2= 60 g; ∆H < 0.
- Resposta e minha dúvida:
Eu até acertei, mas não entendi o ∆H, de nenhuma alternativa, como ele é calculado?





Jigsaw- Monitor

- Mensagens : 636
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
 Re: Questão ITA 2006 - Soluções
Re: Questão ITA 2006 - Soluções
Então independente da forma que eles fizessem os experimentos, o ∆H seria maior que zero, certo? Pois todas essas dissoluções são endotérmicas

Mineira_lanes- Padawan

- Mensagens : 52
Data de inscrição : 02/02/2023
Idade : 20
Localização : MG, Brasil
 Re: Questão ITA 2006 - Soluções
Re: Questão ITA 2006 - Soluções
Mineira_lanes, no caso dos sais apresentados nesse gráfico sim, mas há exceções como no caso do Ce2(SO4)3 onde a dissolução é exotermica (curva descendente):Mineira_lanes escreveu:Então independente da forma que eles fizessem os experimentos, o ∆H seria maior que zero, certo? Pois todas essas dissoluções são endotérmicas

Lembrando que no caso de combustões ocorre exatamente o inverso, são todos processos exotérmicos ∆H<0 (nao me lembro de algum caso de combustão endotérmico).





Jigsaw- Monitor

- Mensagens : 636
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
Mineira_lanes gosta desta mensagem
 Re: Questão ITA 2006 - Soluções
Re: Questão ITA 2006 - Soluções
Jigsaw escreveu:Mineira_lanes, no caso dos sais apresentados nesse gráfico sim, mas há exceções como no caso do Ce2(SO4)3 onde a dissolução é exotermica (curva descendente):Mineira_lanes escreveu:Então independente da forma que eles fizessem os experimentos, o ∆H seria maior que zero, certo? Pois todas essas dissoluções são endotérmicas
Lembrando que no caso de combustões ocorre exatamente o inverso, são todos processos exotérmicos ∆H<0 (nao me lembro de algum caso de combustão endotérmico).


Ficou claro, muito obrigada!

Mineira_lanes- Padawan

- Mensagens : 52
Data de inscrição : 02/02/2023
Idade : 20
Localização : MG, Brasil
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













