Equilíbrio Químico
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equilíbrio Químico
Equilíbrio Químico
O dióxido de nitrogênio (NO₂) é um gás de cor acastanhada, de odor forte e irritante e muito tóxico. É um poderoso oxidante que, nas reações da atmosfera, pode dar origem a ácido nítrico, bem como a nitratos orgânicos que contribuem para fenômenos com elevado impacto ambiental, como as chuvas ácidas e a eutrofização de lagos e rios. Ele pode ser formado nas reações de combustão dos motores a explosão, na queima de querosene ou a partir da reação do monóxido de nitrogênio (NO) com oxigênio (O₂). O NO₂ pode ser decomposto a gás nitrogênio e a gás oxigênio de acordo com a reação:
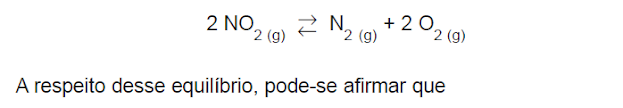
A)o aumento da pressão desloca o equilíbrio no sentido da maior produção de NO₂.
B)o aumento de temperatura, aumenta o valor da constante de equilíbrio da reação.
C)a expressão da velocidade cinética da reação direta é v = k . [NO₂].
D)a adição de catalisador desloca o equilíbrio no sentido da reação direta.
E)por ser um equilíbrio heterogêneo, o aumento da concentração de gás nitrogênio desloca o equilíbrio da reação no sentido de maior formação de O₂.
Gabarito : A
Dúvida : Entendi por que a A está correta, mas gostaria de saber por que a B está incorreta. O texto menciona que o NO2 é formado a partir de reações exotérmicas (combustão) , então assumi que o sentido direto da reação seria, ao contrário do inverso, endotérmico . Nessa linha de raciocínio , o aumento da temperatura aumentaria a constante de equilíbrio, não ?
A)o aumento da pressão desloca o equilíbrio no sentido da maior produção de NO₂.
B)o aumento de temperatura, aumenta o valor da constante de equilíbrio da reação.
C)a expressão da velocidade cinética da reação direta é v = k . [NO₂].
D)a adição de catalisador desloca o equilíbrio no sentido da reação direta.
E)por ser um equilíbrio heterogêneo, o aumento da concentração de gás nitrogênio desloca o equilíbrio da reação no sentido de maior formação de O₂.
Gabarito : A
Dúvida : Entendi por que a A está correta, mas gostaria de saber por que a B está incorreta. O texto menciona que o NO2 é formado a partir de reações exotérmicas (combustão) , então assumi que o sentido direto da reação seria, ao contrário do inverso, endotérmico . Nessa linha de raciocínio , o aumento da temperatura aumentaria a constante de equilíbrio, não ?

girassol2910- Padawan

- Mensagens : 58
Data de inscrição : 16/06/2021
Idade : 19

Markerrzo- Recebeu o sabre de luz

- Mensagens : 159
Data de inscrição : 05/02/2019
Idade : 26
Localização : Rio das Ostras - RJ
marcosprb gosta desta mensagem
 Re: Equilíbrio Químico
Re: Equilíbrio Químico
Oii !
Muito obrigada pela resolução (perfeita, por sinal ) ! Ao ler o enunciado, especialmente a parte da combustão em motores, pensei que a formação do NO2 fosse exotérmica. Agora, sabendo que, de fato, trata-se do sentido endotérmico da reação, acredito que a combustão ceda energia para que haja formação do NO2, certo ?
) ! Ao ler o enunciado, especialmente a parte da combustão em motores, pensei que a formação do NO2 fosse exotérmica. Agora, sabendo que, de fato, trata-se do sentido endotérmico da reação, acredito que a combustão ceda energia para que haja formação do NO2, certo ?
Muito obrigada pela resolução (perfeita, por sinal

girassol2910- Padawan

- Mensagens : 58
Data de inscrição : 16/06/2021
Idade : 19
 Re: Equilíbrio Químico
Re: Equilíbrio Químico
Isso mesmo! A combustão sempre libera (cede) energia, ou seja, é sempre exotérmica com fornecimento de calor.

Markerrzo- Recebeu o sabre de luz

- Mensagens : 159
Data de inscrição : 05/02/2019
Idade : 26
Localização : Rio das Ostras - RJ
girassol2910 gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico - grau de equilíbrio
» equilíbrio químico
» Equilíbrio Químico
» Equilíbrio Químico
» Equilíbrio químico
» equilíbrio químico
» Equilíbrio Químico
» Equilíbrio Químico
» Equilíbrio químico
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














