Gases IME-5 (1989)
4 participantes
PiR2 :: Questões Especiais :: Escolas Militares :: Física
Página 1 de 1
 Gases IME-5 (1989)
Gases IME-5 (1989)
05) (IME-89) Dois recipientes, condutores de calor, de mesmo volume, são interligados por um tubo de volume desprezível e contêm um gás ideal, inicialmente a 23ºC e l,5 x l0^{5} Pa. Um dos recipientes é mergulhado em um líquido a 127ºC, enquanto que o outro, simultaneamente, é mergulhado em oxigênio líquido a - 173ºC. Determine a pressão de equilíbrio do gás.Considere 0ºC = 273 k.
Agash- Recebeu o sabre de luz

- Mensagens : 127
Data de inscrição : 26/07/2011
Idade : 31
Localização : Urca,Rio de Janeiro, Brasil
 Re: Gases IME-5 (1989)
Re: Gases IME-5 (1989)
Confirme o gabarito:
Condições Iniciais:
-> O volume total é: 2V (junção dos dois recipientes)
-> A pressão inicial é Po (1,5x10^5)
-> A temperatura inicial era To [23ºC (296K)]
-> O número de mols era n
Matematicamente:
Pv = n.R.T
n = P.2V/R.To (I)
Condições Finais:
-> O Volume final é 2V (desprezando a dilatação)
-> A Pressão Final é P para ambos os gases (o que procuramos)
-> Volume final é 2V (Sendo V de um gás e V de outro)
-> A temperatura final é diferente para cada gás:
-gás 1: T1 [127ºC (400K)]
-gás 2: T2 [-173ºC (100K)]
-> O número de mols continua sendo n:
Matematicamente:
Para o gás 1:
P.V = n.R.T
n1 = P.V/R.T1 (II)
Para o gás 2:
n2 = P.V/R.T2 (III)
Como o número de mols é constante:
n = n1 + n2 (IV)
Substituindo (I), (II) e (III) em (IV):
P.2V/R.To = P.V/R.T1 P.V/R.T2
Cortando os 'V' e os 'R':
P.2V/R.To = P.V/R.T1 +P.V/R.T2
Substituindo pelos valores dados, e usando latex (haSUHa):
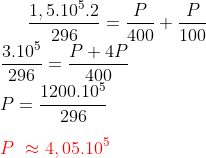
Condições Iniciais:
-> O volume total é: 2V (junção dos dois recipientes)
-> A pressão inicial é Po (1,5x10^5)
-> A temperatura inicial era To [23ºC (296K)]
-> O número de mols era n
Matematicamente:
Pv = n.R.T
n = P.2V/R.To (I)
Condições Finais:
-> O Volume final é 2V (desprezando a dilatação)
-> A Pressão Final é P para ambos os gases (o que procuramos)
-> Volume final é 2V (Sendo V de um gás e V de outro)
-> A temperatura final é diferente para cada gás:
-gás 1: T1 [127ºC (400K)]
-gás 2: T2 [-173ºC (100K)]
-> O número de mols continua sendo n:
Matematicamente:
Para o gás 1:
P.V = n.R.T
n1 = P.V/R.T1 (II)
Para o gás 2:
n2 = P.V/R.T2 (III)
Como o número de mols é constante:
n = n1 + n2 (IV)
Substituindo (I), (II) e (III) em (IV):
P.2V/R.To = P.V/R.T1 P.V/R.T2
Cortando os 'V' e os 'R':
P.2
Substituindo pelos valores dados, e usando latex (haSUHa):

Kongo- Elite Jedi

- Mensagens : 916
Data de inscrição : 22/01/2011
Idade : 30
Localização : Juiz de Fora - MG
 Re: Gases IME-5 (1989)
Re: Gases IME-5 (1989)
Muito bom trabalho Kongo! Beleza.
____________________________________________
In memoriam - Euclides faleceu na madrugada do dia 3 de Abril de 2018.

Lembre-se de que os vestibulares têm provas de Português também! Habitue-se a escrever corretamente em qualquer circunstância!
O Universo das coisas que eu não sei é incomensuravelmente maior do que o pacotinho de coisas que eu penso que sei.
Euclides- Fundador
- Mensagens : 32508
Data de inscrição : 07/07/2009
Idade : 74
Localização : São Paulo - SP
 Re: Gases IME-5 (1989)
Re: Gases IME-5 (1989)
Muito obrigado Kongo!
Então eu sempre fico com dúvida como posso considerar n_1 e n_2 como se estivessem em recipientes separados... Tipo o gás deveria se espalhar por todo o recipiente...
Pelo fato do tubo ter tubo de volume desprezível o gás não se espalha?
Hummm... Fazendo a pergunta acho q entendi a minha dúvida sobre a "mistura" de gases a temperaturas "distintas"... Se um dn de gás da temperatura fosse do recipiente de -173ºC para o de 127ºC me deixou muito intrigado...
Fato que seria possível já que da teoria cinética dos gases,este está em movimento caótico, mas de fato o volume deixado por esse dn que foi para o outro recipiente não ficara "vácuo",ou seja, outra molécula ira ocupar o espaço deixado por aquela, e no fim independente do instante SEMPRE teremos um volume V de gás a 127ºC e outro volume V de gás - 173ºC...
E quando fazemos n_1 e n_2 estamos apenas utilizando um artifício para calcular a pressão em cada recipiente, porque, na verdade, as moléculas do gás determinadas n_1 e n_2 podem deslocar-se pelo recipiente...
AHUHuahU é n_i é a pressão ocasionada pela moléculas presente no recipiente i, que independe do instante e do fato das moléculas poderem se deslocar por TODO o recipiente = ]
Agora sim eu entendi !
Vocês conseguiram perceber onde estava a minha dúvida, acho que não me expressei bem?
Então eu sempre fico com dúvida como posso considerar n_1 e n_2 como se estivessem em recipientes separados... Tipo o gás deveria se espalhar por todo o recipiente...
Pelo fato do tubo ter tubo de volume desprezível o gás não se espalha?
Hummm... Fazendo a pergunta acho q entendi a minha dúvida sobre a "mistura" de gases a temperaturas "distintas"... Se um dn de gás da temperatura fosse do recipiente de -173ºC para o de 127ºC me deixou muito intrigado...
Fato que seria possível já que da teoria cinética dos gases,este está em movimento caótico, mas de fato o volume deixado por esse dn que foi para o outro recipiente não ficara "vácuo",ou seja, outra molécula ira ocupar o espaço deixado por aquela, e no fim independente do instante SEMPRE teremos um volume V de gás a 127ºC e outro volume V de gás - 173ºC...
E quando fazemos n_1 e n_2 estamos apenas utilizando um artifício para calcular a pressão em cada recipiente, porque, na verdade, as moléculas do gás determinadas n_1 e n_2 podem deslocar-se pelo recipiente...
AHUHuahU é n_i é a pressão ocasionada pela moléculas presente no recipiente i, que independe do instante e do fato das moléculas poderem se deslocar por TODO o recipiente = ]
Agora sim eu entendi !
Vocês conseguiram perceber onde estava a minha dúvida, acho que não me expressei bem?
Agash- Recebeu o sabre de luz

- Mensagens : 127
Data de inscrição : 26/07/2011
Idade : 31
Localização : Urca,Rio de Janeiro, Brasil
DerFreieGeist- Iniciante
- Mensagens : 4
Data de inscrição : 21/10/2012
Idade : 30
Localização : Salvador, Bahia, Brasil
PiR2 :: Questões Especiais :: Escolas Militares :: Física
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













