Energia de Ionização
5 participantes
PiR2 :: Física :: Física Moderna
Página 1 de 1
 Energia de Ionização
Energia de Ionização
Para a determinação da 1ª energia de ionização de um determinado elemento químico, forneceu-se uma radiação
eletromagnética de 1152,0 eV ao seu átomo. O elétron foi então ejetado a uma velocidade de 2,0 × 107 m/s. A 1ª energia
de ionização do elemento analisado é de, aproximadamente:
gab.: 1392 kJ/mol
André Albuquerque- Iniciante
- Mensagens : 16
Data de inscrição : 04/07/2013
Idade : 26
Localização : Fortaleza, Ceará, Brasil

Dela Corte- Recebeu o sabre de luz

- Mensagens : 197
Data de inscrição : 31/05/2013
Idade : 26
Localização : Jacareí, São Paulo
 Re: Energia de Ionização
Re: Energia de Ionização
não entendi pq multiplicar o I por 6,02 . 10²³, poderia me explicar, por favor ?
André Albuquerque- Iniciante
- Mensagens : 16
Data de inscrição : 04/07/2013
Idade : 26
Localização : Fortaleza, Ceará, Brasil
 Re: Energia de Ionização
Re: Energia de Ionização
I é a energia de ionização de um átomo. Multiplicando essa energia por 6,02 . 10 ²³ (número de Avogadro), teremos a energia de ionização por mol.

Dela Corte- Recebeu o sabre de luz

- Mensagens : 197
Data de inscrição : 31/05/2013
Idade : 26
Localização : Jacareí, São Paulo
 Re: Energia de Ionização
Re: Energia de Ionização
aaaah, obrigado 
André Albuquerque- Iniciante
- Mensagens : 16
Data de inscrição : 04/07/2013
Idade : 26
Localização : Fortaleza, Ceará, Brasil
 Re: Energia de Ionização
Re: Energia de Ionização
Alguém poderia postar a resolução desse problema?
shady17- Jedi

- Mensagens : 322
Data de inscrição : 23/05/2013
Idade : 32
Localização : Uberlândia MG
 Re: Energia de Ionização
Re: Energia de Ionização
Estou precisando da resolução também!

Augusto H.- Mestre Jedi

- Mensagens : 509
Data de inscrição : 22/03/2017
Idade : 25
Localização : Porto Alegre
 Re: Energia de Ionização
Re: Energia de Ionização
A energia cinética desse fóton será igual a energia total fornecida - a energia de ionização.
Uma das aplicações da Teoria Quântica de Planck resolve esta questão:

ou
 sendo hv energia total ou radiação eletromagnética total absorvida.
sendo hv energia total ou radiação eletromagnética total absorvida.
e
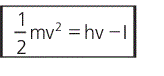 sendo I a energia de ionização.
sendo I a energia de ionização.
então: 1/2mv^2 = 1152,0eV - I
massa do elétron = 9,1095 x10^–31kg
eV =1,6022x10^-19J
Agora é só substituir os valores e ajeitar a equação : )
1152.1,6x10^-19 - (1/2. 9x10^-31. 4x10^14) = I
1843,2x10^-19 - (18,2x10^-17) = I = 2,32x10^-18
Não se esqueça que este valor está relacionado a energia de ionização de um único elétron. Como a resposta está expressa em função de mol, deve-se multiplicar esse I encontrado pela constante de Avogadro.
Por fim, você obterá 6x10^23 . 2,32x10^-18 = 1392kJ/mol
--------------------------------------------------------------------------------------------------------------------------------
Adendo:
Outra forma de se calcular ''I'':
A energia de ionização, para átomos hidrogenoides, pode ser obtida com a equação de Rydberg:
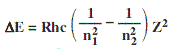
(rhc = constante de Rydberg para o átomo em questão)
(deltaE = diferença de energia entre os níveis n1 e n2)
A remoção completa de um elétron de um átomo pode ser uma forma de ionização, que é efetivamente mover o elétron para um orbital com um número quântico principal infinito.
 Assim deltaE = I
Assim deltaE = I
Entretanto, como não se conhece o número atômico Z e nem o nível n1, a equação não é útil neste caso.
Existem ainda outras formas!!
Uma das aplicações da Teoria Quântica de Planck resolve esta questão:

ou
 sendo hv energia total ou radiação eletromagnética total absorvida.
sendo hv energia total ou radiação eletromagnética total absorvida.e
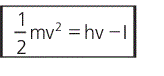 sendo I a energia de ionização.
sendo I a energia de ionização.então: 1/2mv^2 = 1152,0eV - I
massa do elétron = 9,1095 x10^–31kg
eV =1,6022x10^-19J
Agora é só substituir os valores e ajeitar a equação : )
1152.1,6x10^-19 - (1/2. 9x10^-31. 4x10^14) = I
1843,2x10^-19 - (18,2x10^-17) = I = 2,32x10^-18
Não se esqueça que este valor está relacionado a energia de ionização de um único elétron. Como a resposta está expressa em função de mol, deve-se multiplicar esse I encontrado pela constante de Avogadro.
Por fim, você obterá 6x10^23 . 2,32x10^-18 = 1392kJ/mol
--------------------------------------------------------------------------------------------------------------------------------
Adendo:
Outra forma de se calcular ''I'':
A energia de ionização, para átomos hidrogenoides, pode ser obtida com a equação de Rydberg:
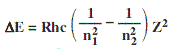
(rhc = constante de Rydberg para o átomo em questão)
(deltaE = diferença de energia entre os níveis n1 e n2)
A remoção completa de um elétron de um átomo pode ser uma forma de ionização, que é efetivamente mover o elétron para um orbital com um número quântico principal infinito.
 Assim deltaE = I
Assim deltaE = IEntretanto, como não se conhece o número atômico Z e nem o nível n1, a equação não é útil neste caso.
Existem ainda outras formas!!

Hume_Mascarenhas- Padawan

- Mensagens : 56
Data de inscrição : 17/01/2018
Idade : 26
Localização : Guarulhos, SP, Brasil.
GuiGui_62 gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Energia de ionização
» Energia de Ionização
» Energia de Ionização
» ENERGIA DE IONIZAÇÃO
» Energia de Ionização
» Energia de Ionização
» Energia de Ionização
» ENERGIA DE IONIZAÇÃO
» Energia de Ionização
PiR2 :: Física :: Física Moderna
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














