Polaridade da molécula H2CO3
4 participantes
Página 2 de 2
Página 2 de 2 •  1, 2
1, 2
 Polaridade da molécula H2CO3
Polaridade da molécula H2CO3
Relembrando a primeira mensagem :
Então pessoal, agora estou com dúvida em relação a polaridade da molécula de H2CO3.
Primeiramente quero explicar o jeito que eu aprendi fazer a polaridade sem precisar fazer os momentos dipolares resultantes:
-Nº de pares de elétrons ao redor do átomo central = Nº de átomos iguais ligados ao átomo central = APOLAR
-Nº de pares de elétrons ao redor do átomo central ≠ Nº de átomos igual ligados ao átomo central = POLAR
OBS: Consideramos duplas e triplas ligações como um par te elétrons.
Ex.: CH4 (4 pares de elétrons ao redor do C = 4 átomos de hidrogênio ligados ao - APOLAR)
NH3 (4 pares de elétrons ao redor no N ≠ 3 átomos de hidrogênio ligados ao N - POLAR)
Em relação ao H2CO3, é uma molécula polar. Porém resolvendo do jeito que aprendi, eu encontrei ela apolar:
3 pares de elétrons ao redor do C = 3 átomos de O ligados ao C - APOLAR

E agora?
Muito obrigado.
Então pessoal, agora estou com dúvida em relação a polaridade da molécula de H2CO3.
Primeiramente quero explicar o jeito que eu aprendi fazer a polaridade sem precisar fazer os momentos dipolares resultantes:
-Nº de pares de elétrons ao redor do átomo central = Nº de átomos iguais ligados ao átomo central = APOLAR
-Nº de pares de elétrons ao redor do átomo central ≠ Nº de átomos igual ligados ao átomo central = POLAR
OBS: Consideramos duplas e triplas ligações como um par te elétrons.
Ex.: CH4 (4 pares de elétrons ao redor do C = 4 átomos de hidrogênio ligados ao - APOLAR)
NH3 (4 pares de elétrons ao redor no N ≠ 3 átomos de hidrogênio ligados ao N - POLAR)
Em relação ao H2CO3, é uma molécula polar. Porém resolvendo do jeito que aprendi, eu encontrei ela apolar:
3 pares de elétrons ao redor do C = 3 átomos de O ligados ao C - APOLAR

E agora?
Muito obrigado.
henriquehdias- Jedi

- Mensagens : 303
Data de inscrição : 19/03/2012
Idade : 33
Localização : Ijuí
 Re: Polaridade da molécula H2CO3
Re: Polaridade da molécula H2CO3
Parte IV
Vamos ver o nosso amigo CO2, O=C=O , que é uma molécula linear:

Onde a resultante, por simetria óbvia, é nula, logo, é APOLAR.
Agora uma pentatômica , um dos componentes de nosso "pum"
, um dos componentes de nosso "pum"  :
:
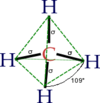
No Metano , CH4, o Carbono é o "fortão", não tanto, mas é o mais eletronegativo dos dois, basta conferir lá na tabela , então atrái os elétrons mais para si.
Mas pela simetria de sua estrutura espacial, os vetores também se anulam: APOLAR.
Finalmente, o seu caso inicial, o H2CO3, o instável ácido carbônico, que está sempre louco para se decompor em H20 e CO2 :geek: !

Percebe-se que a soma de momentos dipolares elétricos não será nula e que a resultante será para cima.
Com as dicas da tabela e se usando o separador de orelhas bem, fica fácil !
Como a polaridade vai depender muito da estrutura espacial e como a estrutura espacil tem "regras" parecidas com as que você citou, pode-se se usar também , "de tabela", as regras para as estruturas moleculares...
Por exemplo, moléculas trigonais como o BF3 , trifluoreto de boro, são apolares pela simetria do triângulo equilátero:

Os vetores momentos se anulam !

Boa Sorte e Bons Estudos :study: :scratch: :study: :bom: :study: !
!
E Vamos Lá !
Vamos ver o nosso amigo CO2, O=C=O , que é uma molécula linear:
Onde a resultante, por simetria óbvia, é nula, logo, é APOLAR.
Agora uma pentatômica
 :
:
No Metano , CH4, o Carbono é o "fortão", não tanto, mas é o mais eletronegativo dos dois, basta conferir lá na tabela , então atrái os elétrons mais para si.
Mas pela simetria de sua estrutura espacial, os vetores também se anulam: APOLAR.
Finalmente, o seu caso inicial, o H2CO3, o instável ácido carbônico, que está sempre louco para se decompor em H20 e CO2 :geek: !
Percebe-se que a soma de momentos dipolares elétricos não será nula e que a resultante será para cima.
Com as dicas da tabela e se usando o separador de orelhas bem, fica fácil !
Como a polaridade vai depender muito da estrutura espacial e como a estrutura espacil tem "regras" parecidas com as que você citou, pode-se se usar também , "de tabela", as regras para as estruturas moleculares...
Por exemplo, moléculas trigonais como o BF3 , trifluoreto de boro, são apolares pela simetria do triângulo equilátero:

Os vetores momentos se anulam !

Boa Sorte e Bons Estudos :study: :scratch: :study: :bom: :study:
E Vamos Lá !
Última edição por rihan em Qua 28 Mar 2012, 14:11, editado 4 vez(es)
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
 Re: Polaridade da molécula H2CO3
Re: Polaridade da molécula H2CO3
Excelente explanação, rihan! Parabéns!
hygorvv- Elite Jedi

- Mensagens : 1721
Data de inscrição : 15/03/2010
Idade : 35
Localização : Vila Velha
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
 Re: Polaridade da molécula H2CO3
Re: Polaridade da molécula H2CO3
Muito obrigado mesmo pela explicação.
Agora eu quero retificar o meu "macete", pois descobri como devo considerar.
Macete/Regra da polaridade:
nº de pares de e- ao redor do átomo central = nº de átomos iguais ligados ao átomo central = APOLAR
nº de pares de e- ao redor do atomo central ≠ nº de atomos iguais ligados ao átomo central = POLAR
OBS.:
-Consideramos duplas e triplas como se fossem um par de elétrons.
-Devemos considerar "átomos iguais" como "grupo de átomos".
Então no caso do H2CO3 temos o "C" ligado a um "O" com dupla e dois "OH" ligados com simples, portanto temos apenas 2 "grupos de átomos" iguais.
Sendo assim, a minha regra funciona para todos os casos e o macete é muito bem-vindo pois simplifica bastante e ajuda na resolução de exercícios de vestibulares.
Agradeço muito pela atenção nessa questão e também me coloco a disposição para crescermos juntos nos conhecimentos.
Agora eu quero retificar o meu "macete", pois descobri como devo considerar.
Macete/Regra da polaridade:
nº de pares de e- ao redor do átomo central = nº de átomos iguais ligados ao átomo central = APOLAR
nº de pares de e- ao redor do atomo central ≠ nº de atomos iguais ligados ao átomo central = POLAR
OBS.:
-Consideramos duplas e triplas como se fossem um par de elétrons.
-Devemos considerar "átomos iguais" como "grupo de átomos".
Então no caso do H2CO3 temos o "C" ligado a um "O" com dupla e dois "OH" ligados com simples, portanto temos apenas 2 "grupos de átomos" iguais.
Sendo assim, a minha regra funciona para todos os casos e o macete é muito bem-vindo pois simplifica bastante e ajuda na resolução de exercícios de vestibulares.
Agradeço muito pela atenção nessa questão e também me coloco a disposição para crescermos juntos nos conhecimentos.
henriquehdias- Jedi

- Mensagens : 303
Data de inscrição : 19/03/2012
Idade : 33
Localização : Ijuí
 Re: Polaridade da molécula H2CO3
Re: Polaridade da molécula H2CO3
As explanações do Mestre rihan são muito agradáveis e divertidas de ver, e tentar entender.Cheias de paciência ,bom humor e casos vividos.
Valeu mestre.
Valeu mestre.

Rafael Ibatexano- Grupo
Velhos amigos do Fórum
- Mensagens : 347
Data de inscrição : 21/09/2009
Localização : IBATÉ-SP
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
Página 2 de 2 •  1, 2
1, 2
 Tópicos semelhantes
Tópicos semelhantes» Molécula
» GEOMETRIA DA MOLECULA
» Massa de uma molécula
» Calcular a molecula
» Hibridização da molécula de N2
» GEOMETRIA DA MOLECULA
» Massa de uma molécula
» Calcular a molecula
» Hibridização da molécula de N2
Página 2 de 2
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













