|Eletroquímica| - Lei de Hess e Potencial de Reação
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 |Eletroquímica| - Lei de Hess e Potencial de Reação
|Eletroquímica| - Lei de Hess e Potencial de Reação
Não estou conseguindo entender uma parte da teoria de Eletroquímica.
O professor afirmou que os potenciais de uma reação NÃO SEGUEM A LEI DE HESS, ou seja: ao somarmos duas equações, não podemos simplesmente somar seus potenciais padrão. Como alternativa, ele sugeriu usar as energias livres de Gibbs, que podem ser calculadas por:
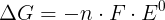
O professor afirmou que os potenciais de uma reação NÃO SEGUEM A LEI DE HESS, ou seja: ao somarmos duas equações, não podemos simplesmente somar seus potenciais padrão. Como alternativa, ele sugeriu usar as energias livres de Gibbs, que podem ser calculadas por:
Somaríamos, portanto, as energias de Gibbs de cada reação e, após termos a reação global, conseguiríamos calcular o seu potencial.
No entanto, ele fez o uso de dois exemplos em seguida em que, em cada um deles, ele seguiu uma lógica diferente:
Alguém conseguiria me dar um norte? Estou bem confuso, pois esse é meu primeiro contato com eletroquímica 
Última edição por Arlindocampos07 em Seg 26 Set 2022, 11:03, editado 1 vez(es)

Arlindocampos07- Mestre Jedi

- Mensagens : 506
Data de inscrição : 22/02/2022
Idade : 20
Localização : Cajazeiras, Paraíba, Brasil
 Re: |Eletroquímica| - Lei de Hess e Potencial de Reação
Re: |Eletroquímica| - Lei de Hess e Potencial de Reação
Só é possível tratar os potenciais de redução da mesma forma que se trata a entalpia (conforme lei de Hess) quando o número de elétrons envolvidos nas reações de oxidação e redução são iguais. Isso ocorre, nesse caso, por conta do cancelamento do fator \(n\):
\[
\Delta G = - n F\Delta E.
\]
Note que o problema do IME aborda justamente o caso em que \(n = 2\) para ambas as reações envolvidas.
\[
\Delta G = - n F\Delta E.
\]
Note que o problema do IME aborda justamente o caso em que \(n = 2\) para ambas as reações envolvidas.

al171- Fera

- Mensagens : 459
Data de inscrição : 14/03/2017
Idade : 22
Localização : SP
Arlindocampos07 gosta desta mensagem
 Re: |Eletroquímica| - Lei de Hess e Potencial de Reação
Re: |Eletroquímica| - Lei de Hess e Potencial de Reação
Perfeito, @al171! Obrigado pela ajuda!al171 escreveu:Só é possível tratar os potenciais de redução da mesma forma que se trata a entalpia (conforme lei de Hess) quando o número de elétrons envolvidos nas reações de oxidação e redução são iguais. Isso ocorre, nesse caso, por conta do cancelamento do fator \(n\):
\[
\Delta G = - n F\Delta E.
\]
Note que o problema do IME aborda justamente o caso em que \(n = 2\) para ambas as reações envolvidas.

Arlindocampos07- Mestre Jedi

- Mensagens : 506
Data de inscrição : 22/02/2022
Idade : 20
Localização : Cajazeiras, Paraíba, Brasil
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|


















