Titulação
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Titulação
Titulação
A titulação é uma técnica muito usada em análises químicas quantitativas com o intuito de determinar a concentração de um reagente. Apesar do surgimento das técnicas instrumentais e do rápido estabelecimento destas como técnicas padrão para diversos procedimentos, as titulometrias volumétricas se mostram presentes, pois, apesar de serem técnicas relativamente antigas, elas representam ainda economia e confiabilidade nas análises laboratoriais, podendo perfeitamente ser utilizadas na quantificação na grande maioria de agentes químicos em diversos segmentos. Existem vários tipos de titulação, dentre as quais a mais comum é a titulação ácidobase. Na medicina, a titulação é utilizada para ajuste da dosagem de medicação com o efeito desejado.
Sabe se que 5,0 mL de ácido sulfúrico de densidade 1,7 g/mL e 73,5 % em massa são diluídos em 50,0 mL em água destilada e, a seguir, são transferidos, quantitativamente, para um balão volumétrico contendo 2,0 g de carbonato de cálcio puro. A mistura resultante foi aquecida, cuidadosamente, à ebulição para eliminar totalmente o gás liberado na reação. Em seguida o volume foi completado para 250,0 mL com adição de água destilada. Após a homogeneização da solução resultante, retirouse dela uma alíquota de 25,0 mL, que foi titulada com uma solução de hidróxido de sódio 0,4 mol/L. O volume de hidróxido de sódio necessário para neutralizar todo o ácido em excesso é de, aproximadamente:
Dados: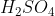 M = 98 g/mol;
M = 98 g/mol; 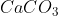 M = 100 g/mol
M = 100 g/mol
Sabe se que 5,0 mL de ácido sulfúrico de densidade 1,7 g/mL e 73,5 % em massa são diluídos em 50,0 mL em água destilada e, a seguir, são transferidos, quantitativamente, para um balão volumétrico contendo 2,0 g de carbonato de cálcio puro. A mistura resultante foi aquecida, cuidadosamente, à ebulição para eliminar totalmente o gás liberado na reação. Em seguida o volume foi completado para 250,0 mL com adição de água destilada. Após a homogeneização da solução resultante, retirouse dela uma alíquota de 25,0 mL, que foi titulada com uma solução de hidróxido de sódio 0,4 mol/L. O volume de hidróxido de sódio necessário para neutralizar todo o ácido em excesso é de, aproximadamente:
Dados:
- RESP:
- 22 ml
matemax- Iniciante
- Mensagens : 21
Data de inscrição : 18/01/2012
Idade : 32
Localização : Natal-RN
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













