Equilíbrio Químico- Porcentagem térmica
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equilíbrio Químico- Porcentagem térmica
Equilíbrio Químico- Porcentagem térmica
3,4 de NH3(g) (17g/mol) são aquecidos a 727 ºC num recipiente indeformável de 0,82 L de capacidade .
Estabelecido o equilíbrio, verifica-se que a pressão total no sistema é igual a 21,2 atm. Calcule a porcentagem de dissociação térmica do NH3 , nas condições acima .
Dados:
Equação de dissociação: 2 NH3(g) ⇄ N2(g) + 3 H2(g)
R = 0,082 atm.L/K.mol
Estabelecido o equilíbrio, verifica-se que a pressão total no sistema é igual a 21,2 atm. Calcule a porcentagem de dissociação térmica do NH3 , nas condições acima .
Dados:
Equação de dissociação: 2 NH3(g) ⇄ N2(g) + 3 H2(g)
R = 0,082 atm.L/K.mol
Carolina.- Jedi

- Mensagens : 266
Data de inscrição : 22/02/2016
Idade : 27
Localização : A. Nogueira - SP -Brasil
 Re: Equilíbrio Químico- Porcentagem térmica
Re: Equilíbrio Químico- Porcentagem térmica
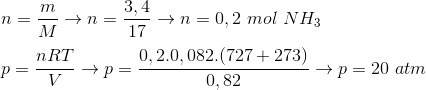


Portanto, 6%.
OBS: Caso você tenha o gabarito, poste-o, pois isso facilita para quem está resolvendo o exercício.

Giovana Martins- Grande Mestre

- Mensagens : 7606
Data de inscrição : 15/05/2015
Idade : 23
Localização : São Paulo
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico - grau de equilíbrio
» Equilíbrio Químico.
» (FCC) Equilíbrio Químico
» Equilíbrio químico
» Equilíbrio Químico
» Equilíbrio Químico.
» (FCC) Equilíbrio Químico
» Equilíbrio químico
» Equilíbrio Químico
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













