Cinética química
Página 1 de 1
 Cinética química
Cinética química
A equação química abaixo representa a hidrólise de alguns dissacarídeos presentes em importantes fontes alimentares:
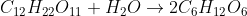
A tabela a seguir relaciona os resultados da velocidade inicial de reação dessa hidrólise, em função da concentração e da temperatura, obtidos em quatro experimentos, sob as seguintes
condições:
- soluções de um desses dissacarídeos foram incubadas com quantidades iguais ora de suco gástrico, ora de suco intestinal rico em enterócitos;
- o tempo de reação e outros possíveis fatores interferentes foram mantidos constantes.

Os experimentos que podem corresponder à hidrólise
enzimática ocorrida quando o dissacarídeo foi incubado com
suco intestinal são os de números:
a) I e II
b) I e IV
c) II e III
d) III e IV
Não entendi! Podem ajudar?
A tabela a seguir relaciona os resultados da velocidade inicial de reação dessa hidrólise, em função da concentração e da temperatura, obtidos em quatro experimentos, sob as seguintes
condições:
- soluções de um desses dissacarídeos foram incubadas com quantidades iguais ora de suco gástrico, ora de suco intestinal rico em enterócitos;
- o tempo de reação e outros possíveis fatores interferentes foram mantidos constantes.

Os experimentos que podem corresponder à hidrólise
enzimática ocorrida quando o dissacarídeo foi incubado com
suco intestinal são os de números:
a) I e II
b) I e IV
c) II e III
d) III e IV
Não entendi! Podem ajudar?
leoamaral- Recebeu o sabre de luz

- Mensagens : 121
Data de inscrição : 25/09/2012
Idade : 33
Localização : BH
 Re: Cinética química
Re: Cinética química
Você precisa ter em mente que a enzima pode desnaturar. E também lembrar que a enzima tem uma capacidade máxima de trabalho.
No experimento 1, conforme aumenta-se a temperatura a enzima vai aumentando sua velocidade de trabalho, até que quando vai aumentando de mais a temperatura, ela vai desnaturando e sua capacidade de trabalho vai diminuindo, conforme o esperado.
No experimento 2, à temperatura constante, a concentração vai aumentando e a velocidade também aumenta, só que a capacidade da enzima vai ter que diminuir, pois sua capacidade de trabalho é limitada. Portanto ela é inconveniente.
No experimento 3, a temperatura aumenta e a velocidade praticamente não aumenta, o que é inviável. Se você reparar, a uma concentração e temperatura 40, a velocidade é 1 u.a. o que não vai de encontro aos outros experimentos.
No experimento 4, no aumento de concentração, a velocidade vai aumentando rapidamente e depois lentamente parecendo chegar num limiar, que é capacidade de trabalho da enzima, o que é esperado.
No experimento 1, conforme aumenta-se a temperatura a enzima vai aumentando sua velocidade de trabalho, até que quando vai aumentando de mais a temperatura, ela vai desnaturando e sua capacidade de trabalho vai diminuindo, conforme o esperado.
No experimento 2, à temperatura constante, a concentração vai aumentando e a velocidade também aumenta, só que a capacidade da enzima vai ter que diminuir, pois sua capacidade de trabalho é limitada. Portanto ela é inconveniente.
No experimento 3, a temperatura aumenta e a velocidade praticamente não aumenta, o que é inviável. Se você reparar, a uma concentração e temperatura 40, a velocidade é 1 u.a. o que não vai de encontro aos outros experimentos.
No experimento 4, no aumento de concentração, a velocidade vai aumentando rapidamente e depois lentamente parecendo chegar num limiar, que é capacidade de trabalho da enzima, o que é esperado.
Convidado- Convidado
 Re: Cinética química
Re: Cinética química
Gabriel,
Confesso que tinha analisado essas situações (concentração, temperatura), porém ainda continuo sem saber como obter a resposta certa.
Realmente no experimento III a temperatura num primeiro momento não interfere muito na velocidade da reação, mas a de 40ºC temos um aumento significativo, e no experimento II temos uma situação muito parecida com o experimento IV.
E agora? Todos relacionam temperatura e concentração!
Poderia me ajudar a entender melhor o exercício!
Confesso que tinha analisado essas situações (concentração, temperatura), porém ainda continuo sem saber como obter a resposta certa.
Realmente no experimento III a temperatura num primeiro momento não interfere muito na velocidade da reação, mas a de 40ºC temos um aumento significativo, e no experimento II temos uma situação muito parecida com o experimento IV.
E agora? Todos relacionam temperatura e concentração!
Poderia me ajudar a entender melhor o exercício!
leoamaral- Recebeu o sabre de luz

- Mensagens : 121
Data de inscrição : 25/09/2012
Idade : 33
Localização : BH
 Re: Cinética química
Re: Cinética química
Não temos um aumento significativo na de 40ºC, ele vai de 0 a 1. Observe que no experimento IV, a velocidade vai atingindo um limite, quanto mais vc vai aumentando a temperatura, menos ela vai diminuindo, tendendo à algum valor. No II, a cada aumento de concentração, a velocidade aumenta a um espaçamento de 10 u.a., o que é contraditório IV, que vai atingindo um valor limite.
Convidado- Convidado
 Re: Cinética química
Re: Cinética química
Gabriel escreveu:Não temos um aumento significativo na de 40ºC, ele vai de 0 a 1.
Desculpe, pois não me expressei bem. Considerando o experimento III como já havia dito inicialmente não temos uma influencia significativa na velocidade. Porém, a partir de 40ºC à 80ºC verifica-se um aumento significativo na velocidade. O que também atenderia a condições mencionadas. Por isso não entendi! Poderia explicar?
Gabriel escreveu:Observe que no experimento IV, a velocidade vai atingindo um limite, quanto mais vc vai aumentando a temperatura, menos ela vai diminuindo, tendendo à algum valor.
No experimento IV a temperatura é mantida constante! Não entendi...?????
Obrigado!
leoamaral- Recebeu o sabre de luz

- Mensagens : 121
Data de inscrição : 25/09/2012
Idade : 33
Localização : BH
 Re: Cinética química
Re: Cinética química
Por que o aumento significativo da temperatura está de acordo com o mencionado? Isso só demonstra o erro: como esse aumento seria feito? do nada?
é uma característica do experimento. o cara simplesmente quis analisar os dados da velocidade com a temperatura constante. nada de mais.
é uma característica do experimento. o cara simplesmente quis analisar os dados da velocidade com a temperatura constante. nada de mais.
Convidado- Convidado
 Tópicos semelhantes
Tópicos semelhantes» Cinética Química - Leis integrais da Cinética
» Cinética Química
» Cinética Química
» UEM - cinética química
» Cinética química
» Cinética Química
» Cinética Química
» UEM - cinética química
» Cinética química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













