estequiometria
2 participantes
Página 1 de 1
 estequiometria
estequiometria
em um reator foram dispostos 560g de monóxido de carbono e 355g de cloro. admitindo-se a reação entre o monóxido de carbono e o cloro com rendimento de 100% da reação e as limitações de reagentes, a massa de fosgênio produzida é de:
dados:
-massas atômicas: C=12u; Cl=35u; O=16u.
-CO+Cl2\rightarrow COCl2 (reação do fosgênio)
dados:
-massas atômicas: C=12u; Cl=35u; O=16u.
-CO+Cl2\rightarrow COCl2 (reação do fosgênio)

kilamniazzz- Iniciante
- Mensagens : 6
Data de inscrição : 16/02/2022
 Re: estequiometria
Re: estequiometria
Olá;
Vamos calcular a relação de monóxido de carbono e cloro, assim podemos determinar quem é o reagente limitante. Pela reação, conclui-se que:

Dos dados no enunciado temos:
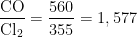
Ou seja, temos muito mais monóxido de carbono do que o necessário, portanto, o cloro é tratado como reagente limitante. Analisando a partir do exposto, podemos determinar a quantidade de fosgênio:
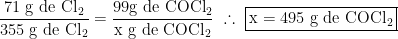
Vamos calcular a relação de monóxido de carbono e cloro, assim podemos determinar quem é o reagente limitante. Pela reação, conclui-se que:
Dos dados no enunciado temos:
Ou seja, temos muito mais monóxido de carbono do que o necessário, portanto, o cloro é tratado como reagente limitante. Analisando a partir do exposto, podemos determinar a quantidade de fosgênio:

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













