Equilíbrios químicos
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equilíbrios químicos
Equilíbrios químicos
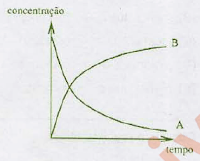
UFRGS 2010 - Observe o gráfico abaixo, no qual a concentração do reagente e do produto de uma reação elementar A --> B foi monitorada em função do tempo.
Assinale a alternativa correta a respeito dessa reação.
(A) A reação ultrapassa o equilíbrio, porque a concentração final do produto é maior do que a do reagente.
(B) A velocidade de desaparecimento de A é sempre igual à velocidade de formação de B.
(C) A velocidade de formação de B torna-se maior que a velocidade de desaparecimento de A após o ponto em que as curvas se cruzam.
(D) A velocidade da reação direta é igual a velocidade da reação inversa no ponto em que as curvas se cruzam.
(E) A lei cinética para essa reação é v = k[A][B]
Resposta: (B)
Dúvida: Por que a letra (B)? Essa reação é reversível?
____________________________________________
"Não se ensina filosofia; ensina-se a filosofar." Immanuel Kant
Acessem: VESTIBULAR EM CASA (https://vestibularemcasa.wixsite.com/vestibularemcasa)
 Re: Equilíbrios químicos
Re: Equilíbrios químicos
Oi,
Então, perceba que as curvas de A e B no gráfico são semelhantes, como elas indicam a variação da concentração em função do tempo, então a velocidade de consumo de A é semelhante a velocidade de formação de B. O que faz perfeito sentido considerando a reação A --> B. Se, por exemplo, 5 mols de A são consumidos por segundo, então 5 mols de B devem se formar por segundo,afinal a matéria não se cria ou se destrói.
Acho que sua confusão reside no conceito de equilíbrio, este acontece quando a velocidade da reação inversa se iguala a velocidade da reação direta, isto é, quando A --> B ocorre na mesma extensão que B --> A.
André Meneses- Recebeu o sabre de luz

- Mensagens : 173
Data de inscrição : 12/07/2016
Idade : 22
Localização : Natal - RN
 Re: Equilíbrios químicos
Re: Equilíbrios químicos
Oi André, boa noite
Acho que entendi...
Tipo, se a reação fosse A --> 2B, então as curvas não seriam simétricas, pois a velocidade de formação de B seria maior do que a do desaparecimento de A, certo?
Acho que entendi...
Tipo, se a reação fosse A --> 2B, então as curvas não seriam simétricas, pois a velocidade de formação de B seria maior do que a do desaparecimento de A, certo?
____________________________________________
"Não se ensina filosofia; ensina-se a filosofar." Immanuel Kant
Acessem: VESTIBULAR EM CASA (https://vestibularemcasa.wixsite.com/vestibularemcasa)
 Re: Equilíbrios químicos
Re: Equilíbrios químicos
Isso mesmo 
André Meneses- Recebeu o sabre de luz

- Mensagens : 173
Data de inscrição : 12/07/2016
Idade : 22
Localização : Natal - RN
 Tópicos semelhantes
Tópicos semelhantes» IME - Equilíbrios Químicos
» IME - Equilíbrios Químicos
» Equilíbrios Químicos
» Equilibrios quimicos
» Atkins - Equilíbrios químicos
» IME - Equilíbrios Químicos
» Equilíbrios Químicos
» Equilibrios quimicos
» Atkins - Equilíbrios químicos
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|