Termodinâmica
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Termodinâmica
Termodinâmica
Uma amostra de n mols de um gás ideal monoatômico é levada do estado de equilíbrio termodinâmico inicial de temperatura Ti até o estado final de equilíbrio de temperatura Tf mediante dois diferentes processos: no primeiro, o volume da amostra permanece constante e ela absorve uma quantidade de calor Qv; no segundo, a pressão da amostra permanece constante e ela absorve uma quantidade de calor Qp. Use a Primeira Lei da Termodinâmica, ∆U=Q-W, sendo ∆U=(3/2)nR∆T, para determinar que se Qp for igual a 100J então o valor de Qv será igual a:
Gab: 60J.
Gab: 60J.

RoddNig- Iniciante
- Mensagens : 29
Data de inscrição : 11/07/2018
Idade : 23
Localização : Brasília
 Re: Termodinâmica
Re: Termodinâmica
Bem, sabemos que em ambos os casos a temperatura foi de T1 a TF consagrando portanto 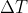
No primeiro caso não há realização de trabalho, pois não há variação de volume, então temos: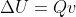 (I)
(I)
No segundo, tendo em vista que a pressão é constante, teremos normalmente que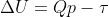 , lembrando, entretanto, que
, lembrando, entretanto, que 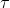 pode ser obtido por P
pode ser obtido por P V, que por sua vez se iguala a
V, que por sua vez se iguala a
NR T, consagrando
T, consagrando 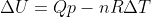 (II)
(II)
Dadas as relações de energia, temos em II que
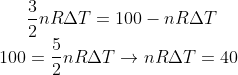 Substituindo em I, teremos :
Substituindo em I, teremos : 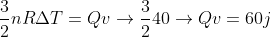
No primeiro caso não há realização de trabalho, pois não há variação de volume, então temos:
No segundo, tendo em vista que a pressão é constante, teremos normalmente que
NR
Dadas as relações de energia, temos em II que

Garrosh- Iniciante
- Mensagens : 5
Data de inscrição : 25/04/2018
Idade : 23
Localização : fortaleza,CE
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













