Cinética!
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Cinética!
Cinética!
A tabela abaixo indica valores das velocidades da reação (v) em três experimentos e as correspondentes concentrações em mol/L dos reagentes X e Y em idênticas condições.
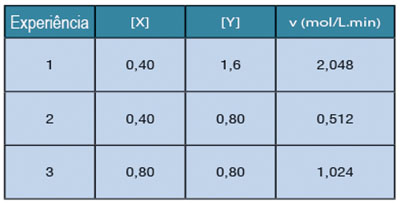
O processo químico é representado pela equação abaixo, na qual a, b e c representam seus coeficientes.
aX +bY ----> cZ
A equação da velocidade desse processo é:

O processo químico é representado pela equação abaixo, na qual a, b e c representam seus coeficientes.
aX +bY ----> cZ
A equação da velocidade desse processo é:
lukassmourafaria- Padawan

- Mensagens : 86
Data de inscrição : 25/04/2015
Idade : 27
Localização : Pouso Alegre/Minas Gerais/Brasil
 Re: Cinética!
Re: Cinética!
Este tópico será movido para: Físico-Química , seu local adequado.
Analisando as experiências 1 e 2:
Como X é constante a velocidade depende apenas da concentração de y, logo se ela aumenta duas vezes, vemos que a velocidade aumenta 4, relação quadrática entre elas:
V = k.[x]^n [y]²
Agora analisando as experiências 2 e 3, a concentração de y é constante e a velocidade nesse caso depende apenas da concentração de x, se x aumentar duas vezes a velocidade também aumenta, relação linear entre elas:
V = k. [x] [y]²
Analisando as experiências 1 e 2:
Como X é constante a velocidade depende apenas da concentração de y, logo se ela aumenta duas vezes, vemos que a velocidade aumenta 4, relação quadrática entre elas:
V = k.[x]^n [y]²
Agora analisando as experiências 2 e 3, a concentração de y é constante e a velocidade nesse caso depende apenas da concentração de x, se x aumentar duas vezes a velocidade também aumenta, relação linear entre elas:
V = k. [x] [y]²
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













