(U. São Judas-SP)
2 participantes
Página 1 de 1
 (U. São Judas-SP)
(U. São Judas-SP)
Quando bebemos água, normalmente a tomamos na forma de goles. Sabendo-se que 1 gole de água ocupa em média o volume de 18 cm³ e que a densidade da água é 1 g/m³ a 4º C, qual o número de moléculas de água ingeridas de cada vez? (Massas atômicas H = 1 u ; O = 16 u)
Achei que a densidade da água fosse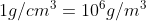 . Usando o valor da densidade do problema em questão, encontrei como resposta
. Usando o valor da densidade do problema em questão, encontrei como resposta 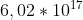 que não bate com o gabarito, entretanto usando valor da densidade que considero como correto, obtém-se a resposta certa, seria um erro de impressão no enunciado? O que vocês acham?
que não bate com o gabarito, entretanto usando valor da densidade que considero como correto, obtém-se a resposta certa, seria um erro de impressão no enunciado? O que vocês acham?
Desde já, muito grato
- Spoiler:
Achei que a densidade da água fosse
Desde já, muito grato
Leandro!- Mestre Jedi

- Mensagens : 963
Data de inscrição : 12/07/2011
Idade : 32
Localização : Rio de Janeiro - RJ
 Re: (U. São Judas-SP)
Re: (U. São Judas-SP)
Densidade da água = 1 g/cm³
Se há 18 cm³ de água, podemos montar a relação:
18 cm³ -- x
1 -- 1
x = 18g
Note que um mol de água tem massa 18g, logo haverá 6,02*10^23 moléculas
Se há 18 cm³ de água, podemos montar a relação:
18 cm³ -- x
1 -- 1
x = 18g
Note que um mol de água tem massa 18g, logo haverá 6,02*10^23 moléculas

JoaoGabriel- Monitor

- Mensagens : 2344
Data de inscrição : 30/09/2010
Idade : 29
Localização : Rio de Janeiro
 Re: (U. São Judas-SP)
Re: (U. São Judas-SP)
Então houve um erro do enunciado ao afirmar que a densidade da água é 1g/m³ e não 1g/cm³.
JoãoGabriel, muito grato pela resolução.
JoãoGabriel, muito grato pela resolução.
Leandro!- Mestre Jedi

- Mensagens : 963
Data de inscrição : 12/07/2011
Idade : 32
Localização : Rio de Janeiro - RJ
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












