Pressão em Transformações Gasosas
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Pressão em Transformações Gasosas
Pressão em Transformações Gasosas
Olá, forumeiros!
Acredito que esta seja minha primeira postagem, e estou com uma dúvida teórica, algo para discutir(mos) e pensar(mos) em como explicar e entender o problema.
Ao pensar em transformações gasosas, e no trabalho realizado em transformações deste tipo, temos que uma abordagem clássica é a transformação sob pressão constante, onde o trabalho é dado pelo produto τ = p.Δv .
Alguns alunos me perguntaram como era possível a pressão se manter constante nesse tipo de transformação.
Eu dei uma explicação, e também mostrei matematicamente a partir da Equação de Clapeyron: pV = n.R.T; se há aumento na temperatura, um aumento proporcional no volume mantém a pressão constante.
Mas senti que eles não ficaram convencidos.
Pensaram em termos de "se aumentamos a temperatura, a energia cinética das partículas aumenta, e o choque com as paredes do recipiente é mais forte. Se é mais forte, tem mais pressão. Ok, o êmbolo pode se movimentar, mas como que isso diminuir a força do impacto?"
Enfim, acredito que era essa a dúvida que tinham. Gostaria de refletir sobre isso, e saber como poderia explicar ou exemplificar algo para sanar esse questionamento, que achei muito pertinente.
Desde já, muito obrigado!
Acredito que esta seja minha primeira postagem, e estou com uma dúvida teórica, algo para discutir(mos) e pensar(mos) em como explicar e entender o problema.
Ao pensar em transformações gasosas, e no trabalho realizado em transformações deste tipo, temos que uma abordagem clássica é a transformação sob pressão constante, onde o trabalho é dado pelo produto τ = p.Δv .
Alguns alunos me perguntaram como era possível a pressão se manter constante nesse tipo de transformação.
Eu dei uma explicação, e também mostrei matematicamente a partir da Equação de Clapeyron: pV = n.R.T; se há aumento na temperatura, um aumento proporcional no volume mantém a pressão constante.
Mas senti que eles não ficaram convencidos.
Pensaram em termos de "se aumentamos a temperatura, a energia cinética das partículas aumenta, e o choque com as paredes do recipiente é mais forte. Se é mais forte, tem mais pressão. Ok, o êmbolo pode se movimentar, mas como que isso diminuir a força do impacto?"
Enfim, acredito que era essa a dúvida que tinham. Gostaria de refletir sobre isso, e saber como poderia explicar ou exemplificar algo para sanar esse questionamento, que achei muito pertinente.
Desde já, muito obrigado!
giu157- Iniciante
- Mensagens : 3
Data de inscrição : 31/10/2016
Idade : 36
Localização : Campinas, São Paulo, Brasil
 Re: Pressão em Transformações Gasosas
Re: Pressão em Transformações Gasosas
Você pode apresentar a dedução da equação τ = p.Δv, já que é derivada dos estudos sobre pressão.
W-> Trabalho(work)
p-> pressão
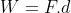 (I)
(I)
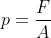
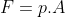 (II)
(II)
II em I ->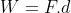 -->
--> 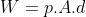
Se em um êmbolo, por exemplo, certa área é deslocada, isso se configura como volume, pois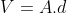
Por isso, chegamos a:
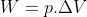
Você pode utilizar a questão sobre choque e energia cinética no sentido de:
Aumentou a temperatura -> aumenta a força das colisões nas paredes do recipiente
Mas... aumentou a força das colisões nas paredes do recipiente -> aumenta o volume -> pressão permanece contante já que p=F/A
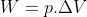
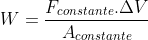
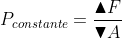
W-> Trabalho(work)
p-> pressão
II em I ->
Se em um êmbolo, por exemplo, certa área é deslocada, isso se configura como volume, pois
Por isso, chegamos a:
Você pode utilizar a questão sobre choque e energia cinética no sentido de:
Aumentou a temperatura -> aumenta a força das colisões nas paredes do recipiente
Mas... aumentou a força das colisões nas paredes do recipiente -> aumenta o volume -> pressão permanece contante já que p=F/A

Dr.Astro- Mestre Jedi

- Mensagens : 516
Data de inscrição : 12/06/2019
Localização : Brasil
 Tópicos semelhantes
Tópicos semelhantes» Transformaçoes gasosas
» Transformações gasosas
» Transformações Gasosas.
» Transformações gasosas
» Transformações gasosas
» Transformações gasosas
» Transformações Gasosas.
» Transformações gasosas
» Transformações gasosas
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












