calorimetria !!
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 calorimetria !!
calorimetria !!
pessoal não é nenhuma questão de cálculos, o q eu quero saber é quando ou quais tipos de problemas devo usar as seguintes fórmulas
|Q | = |Q | e Q + Q = 0
por exemplo essa questão abaixo foi utilizada essa fórmula --> |Q | = |Q | e deu certo, depois tentei utilizar essa Q + Q = 0 e não deu certo, pq ? quais são os tipos de questão q devem ser aplicadas cada uma das fórmulas ??
questão --->
34) Uma piscina contém 1000L de água a temperatura de 22°C. Uma pessoa quer aumentar a temperatura da água da piscina para 25°C, despejando um certo volume de água fervente ( a 100°C ) no interior da mesma .
a) qual é o volume necessário de água fervente ?
b) Sabendo-se que a densidade da água é 1Kg/L , qual é a massa necessária de água fervente ?
1000 L ----> 1 000 kg = 1 000 000 g = 10^6 g
Calor recebido pela água fria: Qr = (10^6)*1*(25 - 22) ----> Qr = 3*10^6 cal
Calor cedido pela massa m de água quente ----> Qc = m*1*(100 - 25) ----> Qc = 75*m cal
|Qc| = |Qr| ----> 75*m = 3*10^6 ----> m = 3 000*10^3/75 ----> m = 40*10^3 g ----> m = 40 kg ----> 40 L
mim ajudem por favor pessoal nessa dúvida !!




|Q | = |Q | e Q + Q = 0
por exemplo essa questão abaixo foi utilizada essa fórmula --> |Q | = |Q | e deu certo, depois tentei utilizar essa Q + Q = 0 e não deu certo, pq ? quais são os tipos de questão q devem ser aplicadas cada uma das fórmulas ??
questão --->
34) Uma piscina contém 1000L de água a temperatura de 22°C. Uma pessoa quer aumentar a temperatura da água da piscina para 25°C, despejando um certo volume de água fervente ( a 100°C ) no interior da mesma .
a) qual é o volume necessário de água fervente ?
b) Sabendo-se que a densidade da água é 1Kg/L , qual é a massa necessária de água fervente ?
1000 L ----> 1 000 kg = 1 000 000 g = 10^6 g
Calor recebido pela água fria: Qr = (10^6)*1*(25 - 22) ----> Qr = 3*10^6 cal
Calor cedido pela massa m de água quente ----> Qc = m*1*(100 - 25) ----> Qc = 75*m cal
|Qc| = |Qr| ----> 75*m = 3*10^6 ----> m = 3 000*10^3/75 ----> m = 40*10^3 g ----> m = 40 kg ----> 40 L
mim ajudem por favor pessoal nessa dúvida !!

alissonsep- Grupo
Velhos amigos do Fórum
- Mensagens : 1523
Data de inscrição : 21/10/2010
Idade : 32
 Re: calorimetria !!
Re: calorimetria !!
Olá alissonsep,
se lhe ensinaram dessa maneira, acho que não foi uma boa escolha porque acaba ficando meio "bitolado" e o aluno fica sem entender o que se passa.
O fundamento de tudo é a Lei da Conservação da Energia. Quando, num sistema fechado como um calorímetro, dois ou mais corpos são colocados, cada um inicialmente a uma temperatura diferente da dos demais, um dos princípios da termodinâmica nos garante que:
"ocorrerão trocas espontâneas de calor, fluindo dos corpos de maior temperatura para os de menor temperatura, até que todos os corpos estejam à mesma temperatura".
ou seja, até que seja alcançado o Equilíbrio Térmico.
A Lei da Conservação da Energia, por sua vez, nos garante que a energia total do sistema não sofrerá variação, isto é, a soma algébrica dos calores cedidos e dos calores recebidos deverá ser igual a zero.
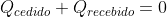
para isso é adotada um convenção algébrica: o calor cedido terá sinal negativo e o calor recebido terá sinal positivo

isso significa que em módulo teremos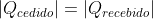 . Lembrando que a variação de temperatura é a diferença: temperatura final - temperatura inicial,
. Lembrando que a variação de temperatura é a diferença: temperatura final - temperatura inicial, 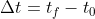 , note que o corpo que se resfriar (temperatura final menor que a inicial) terá uma quantidade de energia com valor negativo. Por isso a sua questão de exemplo e todas as demais podem ser equacionadas assim:
, note que o corpo que se resfriar (temperatura final menor que a inicial) terá uma quantidade de energia com valor negativo. Por isso a sua questão de exemplo e todas as demais podem ser equacionadas assim:
+m_2.c.(t_f-t_0)=0\\\\10^6.1.(25-22)+m.c.(25-100)=0)
se lhe ensinaram dessa maneira, acho que não foi uma boa escolha porque acaba ficando meio "bitolado" e o aluno fica sem entender o que se passa.
O fundamento de tudo é a Lei da Conservação da Energia. Quando, num sistema fechado como um calorímetro, dois ou mais corpos são colocados, cada um inicialmente a uma temperatura diferente da dos demais, um dos princípios da termodinâmica nos garante que:
"ocorrerão trocas espontâneas de calor, fluindo dos corpos de maior temperatura para os de menor temperatura, até que todos os corpos estejam à mesma temperatura".
ou seja, até que seja alcançado o Equilíbrio Térmico.
A Lei da Conservação da Energia, por sua vez, nos garante que a energia total do sistema não sofrerá variação, isto é, a soma algébrica dos calores cedidos e dos calores recebidos deverá ser igual a zero.
para isso é adotada um convenção algébrica: o calor cedido terá sinal negativo e o calor recebido terá sinal positivo
isso significa que em módulo teremos
Última edição por Euclides em Seg 13 Dez 2010, 23:22, editado 2 vez(es)
____________________________________________
In memoriam - Euclides faleceu na madrugada do dia 3 de Abril de 2018.

Lembre-se de que os vestibulares têm provas de Português também! Habitue-se a escrever corretamente em qualquer circunstância!
O Universo das coisas que eu não sei é incomensuravelmente maior do que o pacotinho de coisas que eu penso que sei.
Euclides- Fundador
- Mensagens : 32508
Data de inscrição : 07/07/2009
Idade : 74
Localização : São Paulo - SP
 Re: calorimetria !!
Re: calorimetria !!
brigadão amigo, fico muito satisfeito com a excelente resposta !
então não há, basicamente falando, diferença nenhuma entre as formulas !
vlw
então não há, basicamente falando, diferença nenhuma entre as formulas !
vlw

alissonsep- Grupo
Velhos amigos do Fórum
- Mensagens : 1523
Data de inscrição : 21/10/2010
Idade : 32
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













