(Dúvida na Resolução) - Troca de Calor
+3
aryleudo
Euclides
chrls
7 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 (Dúvida na Resolução) - Troca de Calor
(Dúvida na Resolução) - Troca de Calor
Olá ,
Bem galera.. eu aprendi vendo em uma vídeo aula que uma "forma" mais fácil de resolver exercícios de troca de calor, é:
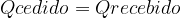
Para calor sensível:
 = m.c.(\Delta \theta final-\theta inicial))
Resolvi várias questões desse modo, por exemplo:
Misturando-se 1,5kg de água a 85°C com 3,0kg de água a 10°C, obtém-se 4,5kg de água à temperatura, em °C, de: (cagua = 1cal/g.°C)
Por esse método:
Como 85°C cede, então:
 = 3000.1.(\theta final-10))
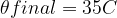
Até ai tudo bem, enquanto as questões eram sobre calor sensível, resolvi todas desse jeito.. porém quando envolveu calor latente eu não consegui... A questão é essa:
(ITA) Inicialmente 48g de gelo a 0ºC são colocados num calorímetro de alumínio de 2,0g, também a 0ºC. Em seguida,
75g de água a 80ºC são despejados dentro desse recipiente. Calcule a temperatura final do conjunto.
Dados: calor latente do gelo Lg = 80cal/g, calor específico da água cH2O = 1,0cal g^(–1)ºC^(–1), calor específico do
alumínio cAl = 0,22cal g^(–1) ºC^(–1).
Seguindo a lógica do que eu tinha aprendido:
 = Mg.Lg + Mal.Cal.(\theta f-\theta i))
 = 48.80 + 2.0,22(\theta f-0))

Porém, o gabarito é: 17,5ºC
Significa então que por esse método não dá pra resolver com calor latente?
Desculpa pela pergunta, pode parecer "boba"... mas não tive isso no 2 grau :/
Obrigado.
Bem galera.. eu aprendi vendo em uma vídeo aula que uma "forma" mais fácil de resolver exercícios de troca de calor, é:
Para calor sensível:
Resolvi várias questões desse modo, por exemplo:
Misturando-se 1,5kg de água a 85°C com 3,0kg de água a 10°C, obtém-se 4,5kg de água à temperatura, em °C, de: (cagua = 1cal/g.°C)
Por esse método:
Como 85°C cede, então:
Até ai tudo bem, enquanto as questões eram sobre calor sensível, resolvi todas desse jeito.. porém quando envolveu calor latente eu não consegui... A questão é essa:
(ITA) Inicialmente 48g de gelo a 0ºC são colocados num calorímetro de alumínio de 2,0g, também a 0ºC. Em seguida,
75g de água a 80ºC são despejados dentro desse recipiente. Calcule a temperatura final do conjunto.
Dados: calor latente do gelo Lg = 80cal/g, calor específico da água cH2O = 1,0cal g^(–1)ºC^(–1), calor específico do
alumínio cAl = 0,22cal g^(–1) ºC^(–1).
Seguindo a lógica do que eu tinha aprendido:
Porém, o gabarito é: 17,5ºC
Significa então que por esse método não dá pra resolver com calor latente?
Desculpa pela pergunta, pode parecer "boba"... mas não tive isso no 2 grau :/
Obrigado.
chrls- Iniciante
- Mensagens : 16
Data de inscrição : 07/04/2010
Idade : 33
Localização : RJ
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
Olá chrls !
O princípio envolvido é a Conservação da Energia. Se temos um sistema fechado (adiabático) como é um calorímetro ideal, ocorrem trocas de calor entre os corpos, mas a energia se conserva, de modo que a soma dos calores cedidos tem de ser igual à soma dos calores recebidos. Como em Calorimetria usualmente designamos calor recebido com um sinal positivo e calor cedido com um sinal negativo, o princípio é geralmente escrito como:
nessa questão onde está a sua dúvida, certamente vale o princípio da conservação da energia. Em questões desse tipo é mais seguro, inicialmente, verificar se a temperatura final estará acima de zero ou será zero. Isto porque de cara podemos não saber se o gelo derrete todo ou não.
O gelo precisará de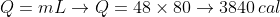 para derreter todo.
para derreter todo.
A água se chegasse a zero grau teria fornecido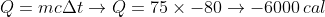 . Isso nos mostra que a temperatura final será mesmo acima de zero.
. Isso nos mostra que a temperatura final será mesmo acima de zero.
Agora precisamos identificar com cuidado as fases do processo:
1) o gelo derrete todo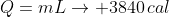
2) a água do gelo derretido agora se aquece) . Você esqueceu desta etapa.
. Você esqueceu desta etapa.
3) o calorímetro se aquece)
4) a água colocada esfria)
Agora vai dar tudo certo.
O princípio envolvido é a Conservação da Energia. Se temos um sistema fechado (adiabático) como é um calorímetro ideal, ocorrem trocas de calor entre os corpos, mas a energia se conserva, de modo que a soma dos calores cedidos tem de ser igual à soma dos calores recebidos. Como em Calorimetria usualmente designamos calor recebido com um sinal positivo e calor cedido com um sinal negativo, o princípio é geralmente escrito como:
nessa questão onde está a sua dúvida, certamente vale o princípio da conservação da energia. Em questões desse tipo é mais seguro, inicialmente, verificar se a temperatura final estará acima de zero ou será zero. Isto porque de cara podemos não saber se o gelo derrete todo ou não.
O gelo precisará de
A água se chegasse a zero grau teria fornecido
Agora precisamos identificar com cuidado as fases do processo:
1) o gelo derrete todo
2) a água do gelo derretido agora se aquece
3) o calorímetro se aquece
4) a água colocada esfria
Agora vai dar tudo certo.
Última edição por Euclides em 23/4/2010, 4:40 pm, editado 1 vez(es)
____________________________________________
In memoriam - Euclides faleceu na madrugada do dia 3 de Abril de 2018.

Lembre-se de que os vestibulares têm provas de Português também! Habitue-se a escrever corretamente em qualquer circunstância!
O Universo das coisas que eu não sei é incomensuravelmente maior do que o pacotinho de coisas que eu penso que sei.
Euclides- Fundador
- Mensagens : 32508
Data de inscrição : 07/07/2009
Idade : 74
Localização : São Paulo - SP
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
Pelo que estou percebendo você só trabalhou com questões onde o calorímetro é ideal, ou seja não há trocas de calor da substância com o calorímetro. Já nessa questão do ITA, em particular, o calorímetro não é ideal. Portanto, o calorímetro também recebe ou perde calor. Compreende?
Você quando armou as contas até considerou que o calorímetro não era ideal, mas não lembro de considerar que o "gelo a 0°C" se derretei totalmente se transformando em "água a 0°C" (Calor Latente). Porém não parou por aí. A "água a 0°C" continua recebendo calor. Acredito que isso foi seu deslise!
Você quando armou as contas até considerou que o calorímetro não era ideal, mas não lembro de considerar que o "gelo a 0°C" se derretei totalmente se transformando em "água a 0°C" (Calor Latente). Porém não parou por aí. A "água a 0°C" continua recebendo calor. Acredito que isso foi seu deslise!
____________________________________________
"Há três coisas na vida que não voltam: As palavras, o tempo e as oportunidades."
Autor Desconhecido

aryleudo- Grande Mestre

- Mensagens : 2292
Data de inscrição : 01/10/2009
Idade : 40
Localização : Cascavel/CE - Brasil
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
montadas essas equações, basta somar todas e igualar a zero, correto ?
thiago.basto- Iniciante
- Mensagens : 29
Data de inscrição : 21/06/2010
Idade : 33
Localização : Bahia
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
____________________________________________
In memoriam - Euclides faleceu na madrugada do dia 3 de Abril de 2018.

Lembre-se de que os vestibulares têm provas de Português também! Habitue-se a escrever corretamente em qualquer circunstância!
O Universo das coisas que eu não sei é incomensuravelmente maior do que o pacotinho de coisas que eu penso que sei.

Euclides- Fundador

- Mensagens : 32508
Data de inscrição : 07/07/2009
Idade : 74
Localização : São Paulo - SP

mhcaf- Padawan

- Mensagens : 90
Data de inscrição : 13/02/2013
Idade : 29
Localização : Recife,PE Brasil
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
Galera, alguem poderia me ajudar com essa questão? Eu entendi todo o processo mas nao entendo como deduzir que o gelo irá derreter.. Ora, o calor nao poderia ir em maior parte para o calorimetro fazendo o gelo nao derreter? Qual o meu erro? Obrigado!
vitorluiz02- Recebeu o sabre de luz

- Mensagens : 132
Data de inscrição : 03/01/2016
Idade : 24
Localização : Palhola, SC, BR
 Re: (Dúvida na Resolução) - Troca de Calor
Re: (Dúvida na Resolução) - Troca de Calor
Basta fazer duas continhas simples
Calor fornecido pela água para chegar a 0 ºC ---> Qa = 75.1.80 ---> Qa = 6 000 cal
Calor recebido para derreter todo o gelo virando água a 0 ºC:
Qg = 48.80 ---> Qg = 3 840 cal
Como Qa > Qg ainda existe muito calor para a água proveniente do gelo (e o calorímetro) aumentar sua temperatura.
Conclusão: todo o gelo virou água
Calor fornecido pela água para chegar a 0 ºC ---> Qa = 75.1.80 ---> Qa = 6 000 cal
Calor recebido para derreter todo o gelo virando água a 0 ºC:
Qg = 48.80 ---> Qg = 3 840 cal
Como Qa > Qg ainda existe muito calor para a água proveniente do gelo (e o calorímetro) aumentar sua temperatura.
Conclusão: todo o gelo virou água

Elcioschin- Grande Mestre

- Mensagens : 71690
Data de inscrição : 15/09/2009
Idade : 77
Localização : Santos/SP
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













