Atomística
2 participantes
Página 1 de 1
 Atomística
Atomística
Ao receber energia, o elétron do átomo de 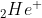 salta da camada L para a camada N. Retornando, o elétron emite uma onda eletromagnética de comprimento de onda λ.
salta da camada L para a camada N. Retornando, o elétron emite uma onda eletromagnética de comprimento de onda λ.
a) Calcule a energia envolvida no salto quântico.
b) Calcule o comprimento de onda da radiação eletromagnética correspondente.
Gabarito:
a) 10,2 eV
b) 121,8 nm
a) Calcule a energia envolvida no salto quântico.
b) Calcule o comprimento de onda da radiação eletromagnética correspondente.
Gabarito:
a) 10,2 eV
b) 121,8 nm
FISMAQUI- Mestre Jedi

- Mensagens : 528
Data de inscrição : 27/05/2011
Idade : 36
Localização : Teresina - PI - Brasil
 Re: Atomística
Re: Atomística
Olá,
Inicialmente, note que:
Camada L → 2° nível (n=2)
Camada N → 4° nível (n=4)
Número atômico do Cátion He+: Z = 2
a)
Utilizando a eq. de Rydberg, têm-se que:
1/λ = RZ²*|1/ni² - 1/nf²| (*hc)
hc/λ = E = hcRZ²*|1/ni² - 1/nf²|
E = (6,67*10^-34)*(3*10^ *(10,9*10^6)*2²*(1/4 - 1/16)
*(10,9*10^6)*2²*(1/4 - 1/16)
E ≈ 16,3*10^-19 J ≈ 10,2 eV.
b)
hc/λ = E
λ = hc/E = (6,67*10^-34)*(3*10^ /(16,3*10^-19)
/(16,3*10^-19)
λ≈122 nm.
Inicialmente, note que:
Camada L → 2° nível (n=2)
Camada N → 4° nível (n=4)
Número atômico do Cátion He+: Z = 2
a)
Utilizando a eq. de Rydberg, têm-se que:
1/λ = RZ²*|1/ni² - 1/nf²| (*hc)
hc/λ = E = hcRZ²*|1/ni² - 1/nf²|
E = (6,67*10^-34)*(3*10^
E ≈ 16,3*10^-19 J ≈ 10,2 eV.
b)
hc/λ = E
λ = hc/E = (6,67*10^-34)*(3*10^
λ≈122 nm.
____________________________________________
Cha-la head-cha-la

Vitor Ahcor- Monitor

- Mensagens : 780
Data de inscrição : 21/12/2018
Idade : 24
Localização : Taurdal
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












