Reações Orgânicas - Ferormônio de Alarme
Página 1 de 1
 Reações Orgânicas - Ferormônio de Alarme
Reações Orgânicas - Ferormônio de Alarme
01. Os pulgões, insetos da família dos afidídeos, que se alimentam de vegetais, aos quais podem transmitir diversas doenças, liberam um ferormônio de alarme, cuja fórmula estrutural está representada a seguir:

A partir da análise da estrutura desse ferormônio, pode-se afirmar:
a) Reage completamente com o hidrogênio, na presença de catalisador, produzindo o alcano 3,7,11-trimetil-dodecano.
b) Descolora algumas gotas de solução de bromo em tetracloreto de carbono.
c) Possui apenas carbonos secundários na estrutura.
d) Absorve energia quando 1 Mol entra em combustão completa, liberando 12 mol de monóxido de carbono.
e) É bastante solúvel em água e apresenta fórmula molecular igual a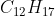 .
.
Tentativa de Resolução;
Pensei numa reação da substância com o bromo, mas não tenho certeza da equação. Caso outro membro responda, gostaria de uma explicação mais detalhada. No caso, mostrando os erros das alternativas ("a", "c", "d" e "e"). Já agradeço.
Gabarito: B

A partir da análise da estrutura desse ferormônio, pode-se afirmar:
a) Reage completamente com o hidrogênio, na presença de catalisador, produzindo o alcano 3,7,11-trimetil-dodecano.
b) Descolora algumas gotas de solução de bromo em tetracloreto de carbono.
c) Possui apenas carbonos secundários na estrutura.
d) Absorve energia quando 1 Mol entra em combustão completa, liberando 12 mol de monóxido de carbono.
e) É bastante solúvel em água e apresenta fórmula molecular igual a
Tentativa de Resolução;
Pensei numa reação da substância com o bromo, mas não tenho certeza da equação. Caso outro membro responda, gostaria de uma explicação mais detalhada. No caso, mostrando os erros das alternativas ("a", "c", "d" e "e"). Já agradeço.
Gabarito: B
Última edição por raimundoocjr em Seg 10 Set 2012, 14:35, editado 1 vez(es)
Convidado- Convidado
 Re: Reações Orgânicas - Ferormônio de Alarme
Re: Reações Orgânicas - Ferormônio de Alarme
(a) O produto deve ser, pelo regra dos menores números, 2,6,10-trimetildodecano.
(b) O chamado "teste do bromo" é utilizado para identificar alcenos e alcinos. As ligações duplas e triplas dos alcenos e dos alcinos, respectivamente, descolorem a solução de bromo em tetracloreto de carbono formando dibrometos ou tetrabrometos que são incolores.
(c) Os carbonos diretamente ligados aos três grupos metil são terciários.
(d) Como há 15 átomos de C nessa molécula, libera 15 mol de CO2.
C15H24 + 21O2 ---> 15CO2 + 12H2O
(e) É pouco solúvel em água pois é uma molécula predominantemente apolar. Além disso, a fórmula molecular é C15H24. Lembre-se que o carbono forma 4 ligações e cada tracinho representa uma ligação com outro átomo de carbono. A(s) ligação(ões) que falta(m) só pode(m) ser com hidrogênio.
(b) O chamado "teste do bromo" é utilizado para identificar alcenos e alcinos. As ligações duplas e triplas dos alcenos e dos alcinos, respectivamente, descolorem a solução de bromo em tetracloreto de carbono formando dibrometos ou tetrabrometos que são incolores.
(c) Os carbonos diretamente ligados aos três grupos metil são terciários.
(d) Como há 15 átomos de C nessa molécula, libera 15 mol de CO2.
C15H24 + 21O2 ---> 15CO2 + 12H2O
(e) É pouco solúvel em água pois é uma molécula predominantemente apolar. Além disso, a fórmula molecular é C15H24. Lembre-se que o carbono forma 4 ligações e cada tracinho representa uma ligação com outro átomo de carbono. A(s) ligação(ões) que falta(m) só pode(m) ser com hidrogênio.
Luís- Estrela Dourada

- Mensagens : 1177
Data de inscrição : 09/02/2011
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













