Gases
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Gases
Gases
. Um dos parâmetros mais importantes no estudo dos gases é o caminho livre médio, representado por . Um gás ideal está confinado em um recipiente de volume V. O número de moléculas desse gás dentro do recipiente é N e o diâmetro de suas moléculas é D. Através de uma dedução por teoria cinética dos gases, o caminho livre médio pode ser calculado por:
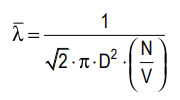
Para 2 mols de gás oxigênio (ideal) ocupando um volume de 100 L a 27º C, calcule:
a) O caminho livre médio;
b) A frequência média de choques entre uma molécula com outras moléculas. Considere que a velocidade modular média é aproximadamente igual a raiz da velocidade quadrática média. O diâmetro das moléculas de gás oxigênio é de 10 2 10 m .
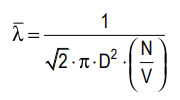
Para 2 mols de gás oxigênio (ideal) ocupando um volume de 100 L a 27º C, calcule:
a) O caminho livre médio;
b) A frequência média de choques entre uma molécula com outras moléculas. Considere que a velocidade modular média é aproximadamente igual a raiz da velocidade quadrática média. O diâmetro das moléculas de gás oxigênio é de 10 2 10 m .
- Spoiler:
- a) 4,69.10-7 m b) Aproximadamente 109 choques/s
Nycolas- Padawan

- Mensagens : 64
Data de inscrição : 19/01/2023
Idade : 19
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













