Lei da Velocidade- Cinética Química
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Lei da Velocidade- Cinética Química
Lei da Velocidade- Cinética Química
A possibilidade de reação de o composto A se transformar no composto B foi estudada em duas condições diferentes. Os gráficos abaixo mostram a concentração de A, em função do tempo, para os experimentos 1 e 2.
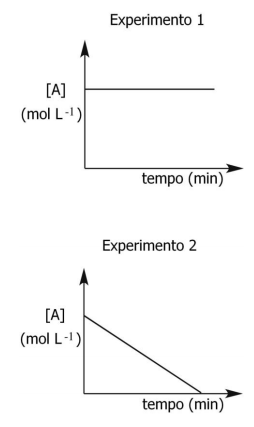
Em relação a esses experimentos, considere as afirmações abaixo.
I - No primeiro experimento, não houve reação.
II - No segundo experimento, a velocidade da reação diminui em função do tempo.
III- No segundo experimento, a reação é de primeira ordem em relação ao composto A.
Quais estão corretas?
(A) Apenas I. (B) Apenas II. (C) Apenas III. (D) Apenas I e III. (E) I, II e III.
Gabarito letra A
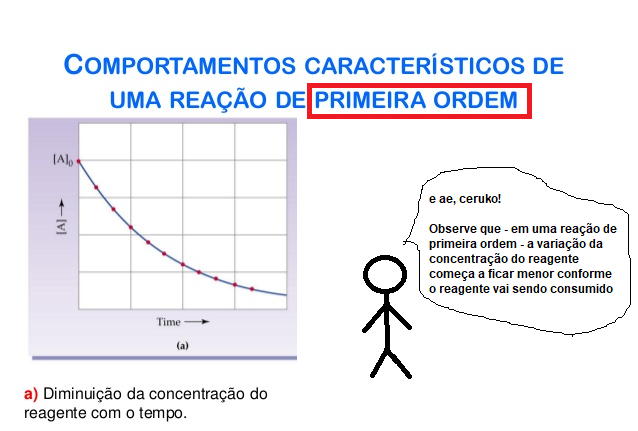
Por que a número 3 está errada? Uma reação de primeira ordem não será um decréscimo constante, como mostrado na figura 2? V= k.(A)¹

Em relação a esses experimentos, considere as afirmações abaixo.
I - No primeiro experimento, não houve reação.
II - No segundo experimento, a velocidade da reação diminui em função do tempo.
III- No segundo experimento, a reação é de primeira ordem em relação ao composto A.
Quais estão corretas?
(A) Apenas I. (B) Apenas II. (C) Apenas III. (D) Apenas I e III. (E) I, II e III.
Gabarito letra A
Por que a número 3 está errada? Uma reação de primeira ordem não será um decréscimo constante, como mostrado na figura 2? V= k.(A)¹

Ceruko- Estrela Dourada

- Mensagens : 1326
Data de inscrição : 01/07/2020
Idade : 23
Localização : Ribeirão Preto
 Re: Lei da Velocidade- Cinética Química
Re: Lei da Velocidade- Cinética Química
Observe que no gráfico 2, qualquer que seja o intervalo de tempo, a relação:
delta[A]
V = ______ é constante.
delta t
Quer dizer que a velocidade NÃO VARIA COM A VARIAÇÃO DA CONCENTRAÇÃO.
Agora compare isso que foi dito com a sua fórmula: V= k.[A]¹
Observe que, de acordo com V= k.[A]¹, a velocidade VARIA COM A VARIAÇÃO DA CONCENTRAÇÃO.
Percebeu?!
A reação 2 é de ordem ZERO
delta[A]
V = ______ é constante.
delta t
Quer dizer que a velocidade NÃO VARIA COM A VARIAÇÃO DA CONCENTRAÇÃO.
Agora compare isso que foi dito com a sua fórmula: V= k.[A]¹
Observe que, de acordo com V= k.[A]¹, a velocidade VARIA COM A VARIAÇÃO DA CONCENTRAÇÃO.
Percebeu?!
A reação 2 é de ordem ZERO
RAFA&L- Estrela Dourada

- Mensagens : 1109
Data de inscrição : 17/10/2019
Idade : 24
Localização : Paraná, Brasil
Ceruko gosta desta mensagem
 Re: Lei da Velocidade- Cinética Química
Re: Lei da Velocidade- Cinética Química
Aliás, essa discussão já existe no site:
https://pir2.forumeiros.com/t154289-cinetica-quimica
https://pir2.forumeiros.com/t154289-cinetica-quimica
RAFA&L- Estrela Dourada

- Mensagens : 1109
Data de inscrição : 17/10/2019
Idade : 24
Localização : Paraná, Brasil
Ceruko gosta desta mensagem
RAFA&L- Estrela Dourada

- Mensagens : 1109
Data de inscrição : 17/10/2019
Idade : 24
Localização : Paraná, Brasil
Ceruko gosta desta mensagem
 Re: Lei da Velocidade- Cinética Química
Re: Lei da Velocidade- Cinética Química
Ahh compreendo agora! Pensei que ordem zero seria somente o gráfico 1, porém, analisando sua explicação, compreendo que se o gráfico for constante, independentemente se o coeficiente linear for diferente de zero (como no gráfico 2 que tem um negativo), esse será de ordem zero! Valeu, amigo.
E, a propósito, adorei o amigo palitinho dando-me uma explicação hahahahaha Muito criativo!
E, a propósito, adorei o amigo palitinho dando-me uma explicação hahahahaha Muito criativo!

Ceruko- Estrela Dourada

- Mensagens : 1326
Data de inscrição : 01/07/2020
Idade : 23
Localização : Ribeirão Preto
 Tópicos semelhantes
Tópicos semelhantes» Lei da Velocidade - Cinética Química
» Cinética quimica-Lei da velocidade
» Questão de Cinética Química (Velocidade)
» |Cinética Química| - Lei de Velocidade (IME/2020 - 2ªF)
» Cinética quimica - Velocidade média
» Cinética quimica-Lei da velocidade
» Questão de Cinética Química (Velocidade)
» |Cinética Química| - Lei de Velocidade (IME/2020 - 2ªF)
» Cinética quimica - Velocidade média
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|