[Resolvido]Reação com a Amônia
2 participantes
Página 1 de 1
![[Resolvido]Reação com a Amônia Empty](https://2img.net/i/empty.gif) [Resolvido]Reação com a Amônia
[Resolvido]Reação com a Amônia
VUNESP
Considere a reação em fase gasosa:
![[Resolvido]Reação com a Amônia 42497548](https://2img.net/r/ihimizer/img215/7108/42497548.png)
Fazendo-se reagir 4L de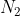 com 9L de
com 9L de 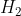 em condições de pressão e temperatura constantes, aponte a alternativa correta e justifique porque as demais estão incorretas.
em condições de pressão e temperatura constantes, aponte a alternativa correta e justifique porque as demais estão incorretas.
![[Resolvido]Reação com a Amônia 57928280](https://2img.net/r/ihimizer/img862/2834/57928280.png)
Gabarito:
Letra "b"
Eu fiz assim:
a) Não sei porque está errada.
![[Resolvido]Reação com a Amônia Eqn4](https://2img.net/r/ihimizer/img683/4276/eqn4.gif)
Galera podem me ajudar no item "a" e "e".
Item "a" -->Não sei
Item "e" ---> Não tenho certeza
Considere a reação em fase gasosa:
![[Resolvido]Reação com a Amônia 42497548](https://2img.net/r/ihimizer/img215/7108/42497548.png)
Fazendo-se reagir 4L de
![[Resolvido]Reação com a Amônia 57928280](https://2img.net/r/ihimizer/img862/2834/57928280.png)
Gabarito:
Letra "b"
Eu fiz assim:
a) Não sei porque está errada.
![[Resolvido]Reação com a Amônia Eqn4](https://2img.net/r/ihimizer/img683/4276/eqn4.gif)
Galera podem me ajudar no item "a" e "e".
Item "a" -->Não sei
Item "e" ---> Não tenho certeza
Última edição por balanar em Seg 18 Abr 2011, 02:55, editado 1 vez(es)

Adam Zunoeta- Monitor

- Mensagens : 4223
Data de inscrição : 25/08/2010
Idade : 35
Localização : Cuiabá
![[Resolvido]Reação com a Amônia Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Reação com a Amônia
Re: [Resolvido]Reação com a Amônia
balanar escreveu:VUNESP
Considere a reação em fase gasosa:
Fazendo-se reagir 4L decom 9L de
em condições de pressão e temperatura constantes, aponte a alternativa correta e justifique porque as demais estão incorretas.
Gabarito:
Letra "b"
Eu fiz assim:
a) Não sei porque está errada.
Galera podem me ajudar no item "a" e "e".
Item "a" -->Não sei
Item "e" ---> Não tenho certeza
Item a: É o seguinte: Avogadro fez uma hipótese: Os gases ideais - principalmente em altas temperaturas e baixas pressões - tem comportamento parecido independente da massa molar. Ou seja, 1 mol de qualquer gás ideal em mesmas temperatura e pressão ocupa o mesmo volume.
N2 e H2 são gases ideais. Assim a proporção em mol pode ser escrita como a proporção em volume.
1 mol de N2 reage com 3 mol de H2
1L de N2 reage com 3L de H2
Multiplicando por 4:
4L de N2 reagem com 12L de H2 e não 9!
A) Está incorreta, N2 está em excesso.
B) N2 está em excesso, seriam necessários 12L de H2 para a reação ser estequiométrica
Correta!
C) Você já percebeu que sobra 1L de N2
Incorreta
D) CUIDADO!
Repare:
1 mol de N2 reage com 3 mol de H2
4 mol de gases reagiram
Foram formados:
2 mol de NH3
2 mol de gases foram formados.
Pela hipótese de Avogadro, os volumes ocupados são diretamente proporcionais ao número de mols.
Se diminui o número de mols, DIMINUI o volume!
Está errado porque não aumenta, diminui o volume.
E)É o seguinte: O H2 é agente limitante
3 mols de H2 formam 2 mols de NH3
3 L de H2 formam 2 L de NH3
Multiplicando por 3:
9 L de H2 formam 6 L de NH3
6L e não 8L.
Incorreta!
Espero ter ajudado!
Abraço

Jean1512- Recebeu o sabre de luz

- Mensagens : 145
Data de inscrição : 08/04/2011
Idade : 32
Localização : Rio de Janeiro RJ |Ipatinga MG
![[Resolvido]Reação com a Amônia Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Reação com a Amônia
Re: [Resolvido]Reação com a Amônia
Show de bola Jean1512.
Vlw Jean1512!

Vlw Jean1512!

Adam Zunoeta- Monitor

- Mensagens : 4223
Data de inscrição : 25/08/2010
Idade : 35
Localização : Cuiabá
 Tópicos semelhantes
Tópicos semelhantes» Produção da amônia
» obtenção do acetato de amônia
» [Resolvido]Reação entre Gases
» Quantidade de amônia
» Formação da amônia
» obtenção do acetato de amônia
» [Resolvido]Reação entre Gases
» Quantidade de amônia
» Formação da amônia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos

![[Resolvido]Reação com a Amônia T3Ri1xW](https://i.imgur.com/T3Ri1xW.png)










