Estequiometria de solução 2
3 participantes
Página 1 de 1
 Estequiometria de solução 2
Estequiometria de solução 2
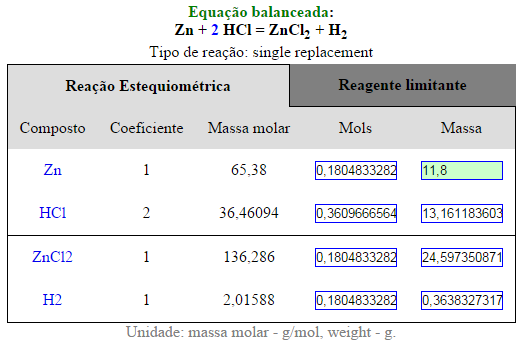
O zinco metálico reage com o HCl aquoso de acordo com a reação:
Zn(s) + HCl(aq) → ZnCl2(s) + H2(g)
Qual o volume de HCl 2,50 mol L-1 é necessário para converter completamente 11,8 g de Zn aos produtos? Zn: 65,39 g mol-1
Zn(s) + HCl(aq) → ZnCl2(s) + H2(g)
Qual o volume de HCl 2,50 mol L-1 é necessário para converter completamente 11,8 g de Zn aos produtos? Zn: 65,39 g mol-1
Jennykah- Jedi

- Mensagens : 286
Data de inscrição : 07/03/2013
Idade : 26
Localização : Juiz de fora, MG
 Re: Estequiometria de solução 2
Re: Estequiometria de solução 2
Eae blz ?
Bom primeiramente balanceando a reação temos que:
Zn(s) + 2HCl(aq) → ZnCl2(s) + H2(g
Agora sabemos que 1 mol de Zn reage com 2 mol de HCl, ou seja como 1 mol de HCl = 36,5 g, 2 mols é 36,5x2 = 73g.
Agora por regra de três temos:
1mol de Zn ---- 2 mol de HCl
0,18 mol de Zn ---- x
x=0,36 mol de HCl
Agora por outra regra de três:
2,50 mol --- 1 L
0,36---- x
x = 0,144 L ou 144ml
Creio que seja isto, um grande abraço!
Bom primeiramente balanceando a reação temos que:
Zn(s) + 2HCl(aq) → ZnCl2(s) + H2(g
Agora sabemos que 1 mol de Zn reage com 2 mol de HCl, ou seja como 1 mol de HCl = 36,5 g, 2 mols é 36,5x2 = 73g.
Agora por regra de três temos:
1mol de Zn ---- 2 mol de HCl
0,18 mol de Zn ---- x
x=0,36 mol de HCl
Agora por outra regra de três:
2,50 mol --- 1 L
0,36---- x
x = 0,144 L ou 144ml
Creio que seja isto, um grande abraço!
Última edição por Shino em Qua 06 Jan 2016, 16:49, editado 1 vez(es)

Shino- Jedi

- Mensagens : 245
Data de inscrição : 18/04/2015
Idade : 26
Localização : Londrina, Paraná.
 Re: Estequiometria de solução 2
Re: Estequiometria de solução 2
Eu não poderia ter feito o passo a passo igual a outra questão que vc me ajudou?
Eu não poderia ter feito assim:
1mol de Zn ---- 73 g de HCl
x mol ------ 11,8
x=0,1616
E disso fazer a relação :
1 mol Zn----2 mol HCl
0,1616--------X
X=0,3232 mol HCl
E então fazer que :
2,50 mol --- 1 L
0,3232 ------x
x=0,1293 L
Por que o primeiro passo que você fez ainda ficou um pouco confuso para mim.
Eu não poderia ter feito assim:
1mol de Zn ---- 73 g de HCl
x mol ------ 11,8
x=0,1616
E disso fazer a relação :
1 mol Zn----2 mol HCl
0,1616--------X
X=0,3232 mol HCl
E então fazer que :
2,50 mol --- 1 L
0,3232 ------x
x=0,1293 L
Por que o primeiro passo que você fez ainda ficou um pouco confuso para mim.
Jennykah- Jedi

- Mensagens : 286
Data de inscrição : 07/03/2013
Idade : 26
Localização : Juiz de fora, MG
 Re: Estequiometria de solução 2
Re: Estequiometria de solução 2
Vc tem o gabarito dessa questão?
Eu faria assim:
2,5mol 0,36mol
-------- = ----------
1000mL x mL
x=144mL
Eu faria assim:

2,5mol 0,36mol
-------- = ----------
1000mL x mL
x=144mL
pedrim27- Mestre Jedi

- Mensagens : 517
Data de inscrição : 30/10/2014
Idade : 25
Localização : Minas Gerais,Brasil
 Re: Estequiometria de solução 2
Re: Estequiometria de solução 2
Bem eu creio que cometi um erro muito feio hahahah. Misturei as unidades .... :evil:, bom foi mal hahaha.
Vamos lá ...
pela reação temos:
1mol de de Zn reage com 2 mol de HCl, porém sabemos que 1 mol de Zn corresponde a 65,39 g, logo podemos montar uma regra de três.
1 mol Zn ----- 2 mol de HCl
65,39 g ------ 2 mol de HCl
11,8 g ----- x mol
fazendo as contas temos que x =0,36 mol de HCl
Como a solução é 2,5 mol ---- 1 L
0,36 mol ---- yL
y = 0,144L ou 144 ml
Peço perdão pelo erro, grande abraço!! Obrigado Pedrim!!!
Vamos lá ...
pela reação temos:
1mol de de Zn reage com 2 mol de HCl, porém sabemos que 1 mol de Zn corresponde a 65,39 g, logo podemos montar uma regra de três.
1 mol Zn ----- 2 mol de HCl
65,39 g ------ 2 mol de HCl
11,8 g ----- x mol
fazendo as contas temos que x =0,36 mol de HCl
Como a solução é 2,5 mol ---- 1 L
0,36 mol ---- yL
y = 0,144L ou 144 ml
Peço perdão pelo erro, grande abraço!! Obrigado Pedrim!!!

Shino- Jedi

- Mensagens : 245
Data de inscrição : 18/04/2015
Idade : 26
Localização : Londrina, Paraná.
 Tópicos semelhantes
Tópicos semelhantes» estequiometria de solução
» Estequiometria
» Fuvest - dissolução de uma solução aquosa ácida através de solução aquosa básica
» Estequiometria
» Estequiometria
» Estequiometria
» Fuvest - dissolução de uma solução aquosa ácida através de solução aquosa básica
» Estequiometria
» Estequiometria
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













