termodinâmica
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 termodinâmica
termodinâmica
Uma pequena quantidade de um gás ideal é mantida
hermeticamente fechada dentro de um cilindro rígido
dotado de um êmbolo. Puxando-se rapidamente o
êmbolo, verifica-se uma diminuição na temperatura do
gás. Em relação à transformação sofrida por este gás,
é verdadeiro afirmar que
a) o volume aumentou, num processo isobárico.
b) a pressão diminuiu, num processo isovolumétrico.
c) o volume aumentou, num processo isotérmico.
d) o volume aumentou proporcionalmente mais do que
a pressão diminuiu.
e) a pressão diminuiu proporcionalmente mais do que
o volume aumentou
só queria saber por que a letra d tá errada?
hermeticamente fechada dentro de um cilindro rígido
dotado de um êmbolo. Puxando-se rapidamente o
êmbolo, verifica-se uma diminuição na temperatura do
gás. Em relação à transformação sofrida por este gás,
é verdadeiro afirmar que
a) o volume aumentou, num processo isobárico.
b) a pressão diminuiu, num processo isovolumétrico.
c) o volume aumentou, num processo isotérmico.
d) o volume aumentou proporcionalmente mais do que
a pressão diminuiu.
e) a pressão diminuiu proporcionalmente mais do que
o volume aumentou
só queria saber por que a letra d tá errada?
thiago ro- Estrela Dourada

- Mensagens : 1236
Data de inscrição : 20/06/2012
Idade : 27
Localização : luís correia
 Re: termodinâmica
Re: termodinâmica
A D está errada porque:
Se o volume aumenta proporcionalmente mais do que a pressão diminui, a temperatura aumenta. E no exercício, temos que a temperatura diminuiu!
Pode-se comprovar isso analisando a equação de estado para gases ideais:


Considere:
 = Aumentou proporcionalmente mais
= Aumentou proporcionalmente mais
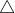 = Aumentou proporcionalmente menos
= Aumentou proporcionalmente menos
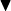 = Diminuiu proporcionalmente mais
= Diminuiu proporcionalmente mais
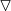 = Diminuiu proporcionalmente menos
= Diminuiu proporcionalmente menos
 = Aumentou a temperatura
= Aumentou a temperatura
 = Diminuiu a temperatura
= Diminuiu a temperatura
-
Demonstração da letra E como certa:
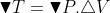
-
OBSERVAÇÃO IMPORTANTE:
Se:
1- A pressão diminuisse proporcionalmente ao que o volume aumentasse,
ou
2- A pressão aumentasse proporcionalmente ao que o volume diminuisse,
A TEMPERATURA CONTINUARIA CONSTANTE
Se o volume aumenta proporcionalmente mais do que a pressão diminui, a temperatura aumenta. E no exercício, temos que a temperatura diminuiu!
Pode-se comprovar isso analisando a equação de estado para gases ideais:
Considere:
-
Demonstração da letra E como certa:
-
OBSERVAÇÃO IMPORTANTE:
Se:
1- A pressão diminuisse proporcionalmente ao que o volume aumentasse,
ou
2- A pressão aumentasse proporcionalmente ao que o volume diminuisse,
A TEMPERATURA CONTINUARIA CONSTANTE
Última edição por GBMED em Qua 29 maio 2013, 19:18, editado 2 vez(es) (Motivo da edição : Informações novas)

GBMED- Iniciante
- Mensagens : 21
Data de inscrição : 06/02/2013
Idade : 29
Localização : Brasil
 Re: termodinâmica
Re: termodinâmica
Valeu!!
thiago ro- Estrela Dourada

- Mensagens : 1236
Data de inscrição : 20/06/2012
Idade : 27
Localização : luís correia
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













