UEM inverno 2016
2 participantes
Página 1 de 1
 UEM inverno 2016
UEM inverno 2016
08) Um prego de massa 10 g aquecido a 100 oC tem mais calor do que a água de uma piscina com 1000 L a 10 oC. 16) Ao nível do mar, a água pura a -4 oC apresenta-se no estado sólido. Contudo, mediante uma redução de pressão, ela pode sofrer fusão
No gabarito, essas afirmações estão como erradas. Alguém poderia me explicar o porquê? Obrigada!
No gabarito, essas afirmações estão como erradas. Alguém poderia me explicar o porquê? Obrigada!
Última edição por annaluiza_y em Ter 30 Jan 2024, 09:52, editado 1 vez(es)

annaluiza_y- Padawan

- Mensagens : 53
Data de inscrição : 21/09/2022
Localização : Londrina-PR
 Re: UEM inverno 2016
Re: UEM inverno 2016
Acredito que o exercício não tenha te dado calor específico e derivados, então vou trabalhar sem essas informações.
08) Um prego de massa 10 g aquecido a 100 oC tem mais calor do que a água de uma piscina com 1000 L a 10 oC.
Calor mede-se de várias formas, mas vamos pensar na fórmula Q=m.c.∆T
Como foi dito que o prego foi aquecido, vamos definir uma temperatura Ti
"Ah,mas o exercício não dá tal valor"
Como a função de Q é linear (O ∆T é elevado a primeira), torna-se uma reta, o que faz com que a mudança da Ti, só defina que região da reta dos valores de Q iremos pegar, e variando, pois estamos olhando para o ∆T, ele define que pedaço da reta pegaríamos.
Prego: Q=10.c.100
Q= 1000c
Água: Q= 1000.1000.c'.10 (medida em gramas para a massa de ambos)
Q=10000000c'
Ou seja, para o prego ter mais calor que a piscina, o calor específico dele teria que ser 10 000 vezes maior que o da água, o que é impossível que um material tenha isso.
Para fins de exemplificação, o c do ferro é de 0,114cal/g.°C e o da água é 1cal/g°C
16) Ao nível do mar, a água pura a -4 oC apresenta-se no estado sólido. Contudo, mediante uma redução de pressão, ela pode sofrer fusão
Ao nível do mar, tem-se 1atm de pressão, e o que nos dá os pontos de fusão e vaporização da água, (0°C e 100°C)
Ou seja, a água pura ao nível do mar e a em -4°C encontra-se solidificada.
Agora vamos para a parte errada:
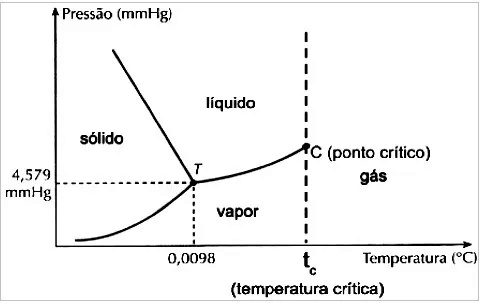
fonte: https://www.manualdaquimica.com/fisico-quimica/o-diagrama-fases.htm
O diagrama de fases é essencial pra que entenda-se o que ocorre, se abaixarmos a pressão da água no estado sólido, é possível perceber pelo diagrama que, com a temperatura mantida, ela irá continuar sólida.
08) Um prego de massa 10 g aquecido a 100 oC tem mais calor do que a água de uma piscina com 1000 L a 10 oC.
Calor mede-se de várias formas, mas vamos pensar na fórmula Q=m.c.∆T
Como foi dito que o prego foi aquecido, vamos definir uma temperatura Ti
"Ah,mas o exercício não dá tal valor"
Como a função de Q é linear (O ∆T é elevado a primeira), torna-se uma reta, o que faz com que a mudança da Ti, só defina que região da reta dos valores de Q iremos pegar, e variando, pois estamos olhando para o ∆T, ele define que pedaço da reta pegaríamos.
Prego: Q=10.c.100
Q= 1000c
Água: Q= 1000.1000.c'.10 (medida em gramas para a massa de ambos)
Q=10000000c'
Ou seja, para o prego ter mais calor que a piscina, o calor específico dele teria que ser 10 000 vezes maior que o da água, o que é impossível que um material tenha isso.
Para fins de exemplificação, o c do ferro é de 0,114cal/g.°C e o da água é 1cal/g°C
16) Ao nível do mar, a água pura a -4 oC apresenta-se no estado sólido. Contudo, mediante uma redução de pressão, ela pode sofrer fusão
Ao nível do mar, tem-se 1atm de pressão, e o que nos dá os pontos de fusão e vaporização da água, (0°C e 100°C)
Ou seja, a água pura ao nível do mar e a em -4°C encontra-se solidificada.
Agora vamos para a parte errada:

fonte: https://www.manualdaquimica.com/fisico-quimica/o-diagrama-fases.htm
O diagrama de fases é essencial pra que entenda-se o que ocorre, se abaixarmos a pressão da água no estado sólido, é possível perceber pelo diagrama que, com a temperatura mantida, ela irá continuar sólida.

Senhor_Regis- Iniciante
- Mensagens : 32
Data de inscrição : 11/01/2024
Localização : São Paulo, SP
 Tópicos semelhantes
Tópicos semelhantes» UEM Inverno 2016
» PUCPR 2016 VESTIBULAR DE INVERNO
» UEM Inverno 2016 Química - Reações Orgânicas
» Dúvida projétil FPP Inverno Medicina 2016
» PUC 2011 Inverno
» PUCPR 2016 VESTIBULAR DE INVERNO
» UEM Inverno 2016 Química - Reações Orgânicas
» Dúvida projétil FPP Inverno Medicina 2016
» PUC 2011 Inverno
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













