Litros de Gás (nitrato de amônio)
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Litros de Gás (nitrato de amônio)
Litros de Gás (nitrato de amônio)
O número total de litros de gás que é gerado quando 1 kg de nitrato de amônio, NH4NO3, a 25 °C e a 1 atm explode, gerando vapor d'água, gás nitrogênio e gás oxigênio (considerando que gases gerados se comportam como gases ideais), é de aproximadamente
Dados :
Massas molares (g mol-1): H = 1; N = 14; O = 16
R = 0,082 L atm mol-1 K-1
0 °C = 273 k
(A) 2,4 (B) 171 (C) 305 (D) 869 (E) 1069
Gab.: E
Dados :
Massas molares (g mol-1): H = 1; N = 14; O = 16
R = 0,082 L atm mol-1 K-1
0 °C = 273 k
(A) 2,4 (B) 171 (C) 305 (D) 869 (E) 1069
Gab.: E
Matheus010- Padawan

- Mensagens : 84
Data de inscrição : 13/05/2015
Idade : 27
 Re: Litros de Gás (nitrato de amônio)
Re: Litros de Gás (nitrato de amônio)
Olá Matheus;
A primeira coisa a se fazer em uma reação química é montá-la e fazer a proporção estequiométrica, assim:

Note que a reação não acontece nas condições normais de pressão e temperatura (CNTP), dessa forma, não podemos afirmar que o volume de 1 mol de um gás qualquer possui 22,4 L. Vamos determinar o volume de um gás nessas mesmas condições, pressão de 1 atm e 25°C, pela Equação de Clapeyron temos:
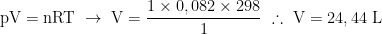
Com o volume determinado, agora sim podemos calcular a quantidade de gases produzidos, fazendo as devidas proporções estequiométricas, dessa forma:
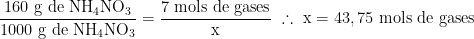
Estabelecemos anteriormente que a cada mol de gás temos um volume ocupado por 24,44 L, logo, em 43,75 mols de gases temos respectivamente:
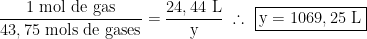
Aproximadamente letra (E).
A primeira coisa a se fazer em uma reação química é montá-la e fazer a proporção estequiométrica, assim:
Note que a reação não acontece nas condições normais de pressão e temperatura (CNTP), dessa forma, não podemos afirmar que o volume de 1 mol de um gás qualquer possui 22,4 L. Vamos determinar o volume de um gás nessas mesmas condições, pressão de 1 atm e 25°C, pela Equação de Clapeyron temos:
Com o volume determinado, agora sim podemos calcular a quantidade de gases produzidos, fazendo as devidas proporções estequiométricas, dessa forma:
Estabelecemos anteriormente que a cada mol de gás temos um volume ocupado por 24,44 L, logo, em 43,75 mols de gases temos respectivamente:
Aproximadamente letra (E).

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
 Tópicos semelhantes
Tópicos semelhantes» Nitrato de amônio
» (UERJ-RJ) - Explosivos, Nitrato de amônio
» Determine quantos litros de água são deslocados, quantos litros de gasolina ficam acima do nível da água...
» Nitrato
» Solubilidade do Nitrato de Prata
» (UERJ-RJ) - Explosivos, Nitrato de amônio
» Determine quantos litros de água são deslocados, quantos litros de gasolina ficam acima do nível da água...
» Nitrato
» Solubilidade do Nitrato de Prata
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













