Propriedades coligativas - ebulioscopia
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Propriedades coligativas - ebulioscopia
Propriedades coligativas - ebulioscopia
(Unimontes-MG–2009) A temperatura de ebulição da água, a 760 mmHg (T.E.), é 100 ºC, e algumas de suas soluções apresentam valores de T.E. mostrados na tabela a seguir:
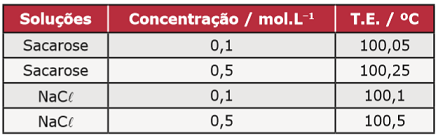
A análise dos dados da tabela revela que
A) o aumento da temperatura de ebulição depende da natureza química do soluto.
B) o número de partículas em solução não influencia na temperatura de ebulição.
C) as moléculas de água em solução passam mais facilmente para o estado gasoso.
D) o valor de ΔT.E. é maior nas soluções de substâncias contendo ligações covalentes.
Bom, eu não estou concordando com a resposta dessa questão. Ao meu ver, no caso de soluções, a temperatura de ebulição depende somente do número de partículas dissolvidas.
No caso dessa questão, comparando 0,1 mol de sacarose com 0,1 mol de NaCl, por exemplo. O NaCl sofre dissociação, por isso o seu número de partículas será maior, nessa caso, 0,2 mol de partículas. Mas 0,3 mol de sacarose, por exemplo, aumenta mais o ponto de ebulição em relação aos 0,1 mol de NaCl.
Por isso acho meio relativo falar que depende da natureza química do soluto.
O que vocês acham ?

A análise dos dados da tabela revela que
A) o aumento da temperatura de ebulição depende da natureza química do soluto.
B) o número de partículas em solução não influencia na temperatura de ebulição.
C) as moléculas de água em solução passam mais facilmente para o estado gasoso.
D) o valor de ΔT.E. é maior nas soluções de substâncias contendo ligações covalentes.
Bom, eu não estou concordando com a resposta dessa questão. Ao meu ver, no caso de soluções, a temperatura de ebulição depende somente do número de partículas dissolvidas.
No caso dessa questão, comparando 0,1 mol de sacarose com 0,1 mol de NaCl, por exemplo. O NaCl sofre dissociação, por isso o seu número de partículas será maior, nessa caso, 0,2 mol de partículas. Mas 0,3 mol de sacarose, por exemplo, aumenta mais o ponto de ebulição em relação aos 0,1 mol de NaCl.
Por isso acho meio relativo falar que depende da natureza química do soluto.
O que vocês acham ?
hugo araujo- Estrela Dourada

- Mensagens : 1758
Data de inscrição : 12/04/2014
Idade : 29
Localização : Araçuaí, MG
 Re: Propriedades coligativas - ebulioscopia
Re: Propriedades coligativas - ebulioscopia
Concordo.
São todas falsas.
São todas falsas.
____________________________________________
"Death is so terribly final, while life is full of possibilities." - Tyrion Lannister
 Re: Propriedades coligativas - ebulioscopia
Re: Propriedades coligativas - ebulioscopia
Obrigado, Pré-Iteano.
hugo araujo- Estrela Dourada

- Mensagens : 1758
Data de inscrição : 12/04/2014
Idade : 29
Localização : Araçuaí, MG
 GRÁFICO INDICA, SIM, O "PESO" DA NATUREZA DO SOLUTO
GRÁFICO INDICA, SIM, O "PESO" DA NATUREZA DO SOLUTO
Olá!
A postagem da questão já é um tanto antiga (considerando a época da minha contribuição), mas acredito ainda ser útil respondê-la.
1) OBSERVEI QUE O GRÁFICO DA QUESTÃO NÃO MOSTRA A DIFERENÇA ENTRE AS CONFIGURAÇÕES DAS TEMPERATURAS DE EBULIÇÃO DO LÍQUIDO PURO E DE UMA POSSÍVEL SOLUÇÃO CONTENTO ESSE LÍQUIDO, MAS DE DUAS SOLUÇÕES DIFERENTES.
*Isso muda tudo, visto que as propriedades coligativas indicam justamente como a adição de um soluto não-volátil influencia em certas características do líquido puro original (que também é o solvente das soluções).
2) COM ESSE PRESSUPOSTO, NÃO CONSIDEREI A MÁXIMA "O AUMENTO DA TEMPERATURA DE EBULIÇÃO NÃO DEPENDE DA NATUREZA DO SOLUTO", UMA VEZ QUE ISSO DESCARTARIA A OBSERVAÇÃO DO GRÁFICO.
*O gráfico da questão mostra que, se se considerar apenas as duas soluções mostradas, de sacarose, um composto molecular, e de cloreto de sódio, um composto iônico, observar-se-á que um deles modifica a temperatura de ebulição da sua solução de uma maneira diferente do outro soluto. No caso estudado, a solução de cloreto de sódio (novamente, um composto iônico) aumenta em 0,4 a temperatura de ebulição [da solução em si] e a solução de sacarose (mais uma vez, um composto molecular), em 0,2. Portanto, há, de fato, uma diferença de variação causada pela natureza do soluto.
Creio ser esse o raciocínio que a questão deseja.
A postagem da questão já é um tanto antiga (considerando a época da minha contribuição), mas acredito ainda ser útil respondê-la.
1) OBSERVEI QUE O GRÁFICO DA QUESTÃO NÃO MOSTRA A DIFERENÇA ENTRE AS CONFIGURAÇÕES DAS TEMPERATURAS DE EBULIÇÃO DO LÍQUIDO PURO E DE UMA POSSÍVEL SOLUÇÃO CONTENTO ESSE LÍQUIDO, MAS DE DUAS SOLUÇÕES DIFERENTES.
*Isso muda tudo, visto que as propriedades coligativas indicam justamente como a adição de um soluto não-volátil influencia em certas características do líquido puro original (que também é o solvente das soluções).
2) COM ESSE PRESSUPOSTO, NÃO CONSIDEREI A MÁXIMA "O AUMENTO DA TEMPERATURA DE EBULIÇÃO NÃO DEPENDE DA NATUREZA DO SOLUTO", UMA VEZ QUE ISSO DESCARTARIA A OBSERVAÇÃO DO GRÁFICO.
*O gráfico da questão mostra que, se se considerar apenas as duas soluções mostradas, de sacarose, um composto molecular, e de cloreto de sódio, um composto iônico, observar-se-á que um deles modifica a temperatura de ebulição da sua solução de uma maneira diferente do outro soluto. No caso estudado, a solução de cloreto de sódio (novamente, um composto iônico) aumenta em 0,4 a temperatura de ebulição [da solução em si] e a solução de sacarose (mais uma vez, um composto molecular), em 0,2. Portanto, há, de fato, uma diferença de variação causada pela natureza do soluto.
Creio ser esse o raciocínio que a questão deseja.
visava5- Iniciante
- Mensagens : 1
Data de inscrição : 02/06/2020
 Tópicos semelhantes
Tópicos semelhantes» Propriedades coligativas
» Propriedades coligativas
» Propriedades coligativas
» Propriedades coligativas
» Propriedades Coligativas.II
» Propriedades coligativas
» Propriedades coligativas
» Propriedades coligativas
» Propriedades Coligativas.II
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














