Radicais
2 participantes
Página 1 de 1
 Re: RADICAIS
Re: RADICAIS
Fala, Ana.
São átomos ou um conjunto de átomos os quais possuem elétrons desemparelhados, também é comum o termo ''valência livre''.
Aprofundando um pouco mais, podemos dizer que esse elétron está sozinho em um orbital atômico.
Além disso, é importante frisar que esses elétrons desemparelhados são, com raras exceções, muito instáveis e altamente reativos, sendo muito bem analisados em reações orgânicas e surgem da cisão homolítica das ligações.
Olhe esse exemplo bem famoso, ainda fica de revisão para as reações de markovnikov:
Sabemos que em reações de adição de alcenos com ácidos da forma HX, ''o hidrogênio é adicionado ao carbono com mais hidrogênios'', mas por quê?
Vou usar o exemplo do propeno reagindo com o HBr, o qual por cisão heterolítica forma H+ e Br-.
Assim:

O H+ ataca a ligação pi (fraca) podendo gerar dois intermediários, no entanto o carbocátion destacado possui mais estabilidade, pois os carbonos vizinhos são doadores de elétrons por efeito indutivo, logo o intermediário da esquerda segue um caminho de menor energia de ativação e é gerado majoritariamente. Após isso, o Br- se liga ao carbono positivo.
Agora, sabemos que ao reagir os mesmos reagentes com um peróxido no meio, acontece justamente o contrário, o hidrogênio é doado ao carbono com menos hidrogênio. Presta atenção:
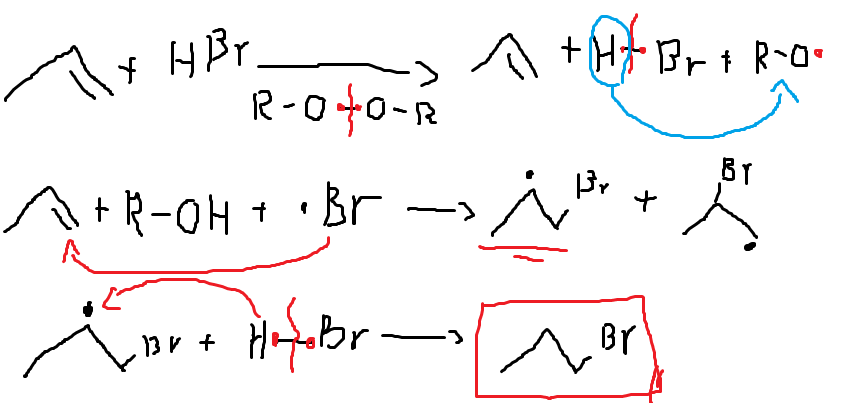
A ligação O-O é fraca e gera dois radicais por cisão homolítica (não há diferença de eletronegatividade entre os 2 oxigênios), esses radicais reagem com o HBr formando um álcool e o radical Br. o qual, posteriormente, reage com o alceno e, por causa do enorme volume do bromo, fica em posições menos substituídas. Nesse caso acontece o famoso Efeito Kharasch, no qual uma reação de adição que, no caso anterior era eletrofílica, torna-se radicalar.
São átomos ou um conjunto de átomos os quais possuem elétrons desemparelhados, também é comum o termo ''valência livre''.
Aprofundando um pouco mais, podemos dizer que esse elétron está sozinho em um orbital atômico.
Além disso, é importante frisar que esses elétrons desemparelhados são, com raras exceções, muito instáveis e altamente reativos, sendo muito bem analisados em reações orgânicas e surgem da cisão homolítica das ligações.
Olhe esse exemplo bem famoso, ainda fica de revisão para as reações de markovnikov:
Sabemos que em reações de adição de alcenos com ácidos da forma HX, ''o hidrogênio é adicionado ao carbono com mais hidrogênios'', mas por quê?
Vou usar o exemplo do propeno reagindo com o HBr, o qual por cisão heterolítica forma H+ e Br-.
Assim:

O H+ ataca a ligação pi (fraca) podendo gerar dois intermediários, no entanto o carbocátion destacado possui mais estabilidade, pois os carbonos vizinhos são doadores de elétrons por efeito indutivo, logo o intermediário da esquerda segue um caminho de menor energia de ativação e é gerado majoritariamente. Após isso, o Br- se liga ao carbono positivo.
Agora, sabemos que ao reagir os mesmos reagentes com um peróxido no meio, acontece justamente o contrário, o hidrogênio é doado ao carbono com menos hidrogênio. Presta atenção:

A ligação O-O é fraca e gera dois radicais por cisão homolítica (não há diferença de eletronegatividade entre os 2 oxigênios), esses radicais reagem com o HBr formando um álcool e o radical Br. o qual, posteriormente, reage com o alceno e, por causa do enorme volume do bromo, fica em posições menos substituídas. Nesse caso acontece o famoso Efeito Kharasch, no qual uma reação de adição que, no caso anterior era eletrofílica, torna-se radicalar.
João Pedro Lima- Jedi

- Mensagens : 218
Data de inscrição : 02/01/2022
Idade : 21
Localização : Rio de Janeiro, RJ
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














