Reação de Neutralização
2 participantes
Página 1 de 1
 Reação de Neutralização
Reação de Neutralização
(UNESP–2006) A amônia (NH3) pode ser biologicamente
produzida, sendo encontrada em excrementos de seres
humanos e de outros animais. Esta substância apresenta
caráter alcalino, podendo reagir com outros gases
presentes na atmosfera, responsáveis pela chuva
ácida. As reações de neutralização desta base com
os ácidos sulfúrico (H2SO4) e nítrico (HNO3) produzem,
respectivamente, os sais
A) NH3HSO4 e NH3NO3.
B) NH3HSO3 e (NH3)2NO2.
C) (NH4)2SO3 e NH4NO3.
D) (NH4)2SO4 e NH4(NO2)2.
E) (NH4)2SO4 e NH4NO3.
Gente, como eu sei quem vai se combinar com o que? Que o NH3, por exemplo, vai virar NH4? Estou muito perdida nesse sentido. O gabarito é letra E
produzida, sendo encontrada em excrementos de seres
humanos e de outros animais. Esta substância apresenta
caráter alcalino, podendo reagir com outros gases
presentes na atmosfera, responsáveis pela chuva
ácida. As reações de neutralização desta base com
os ácidos sulfúrico (H2SO4) e nítrico (HNO3) produzem,
respectivamente, os sais
A) NH3HSO4 e NH3NO3.
B) NH3HSO3 e (NH3)2NO2.
C) (NH4)2SO3 e NH4NO3.
D) (NH4)2SO4 e NH4(NO2)2.
E) (NH4)2SO4 e NH4NO3.
Gente, como eu sei quem vai se combinar com o que? Que o NH3, por exemplo, vai virar NH4? Estou muito perdida nesse sentido. O gabarito é letra E
Última edição por dudinhamedicina2 em Qua 03 Jul 2019, 18:36, editado 2 vez(es)

dudinhamedicina2- Padawan

- Mensagens : 74
Data de inscrição : 06/06/2019
Idade : 26
Localização : Delmiro Gouveia, Alagoas, Brasil
 Re: Reação de Neutralização
Re: Reação de Neutralização
Vamos por partes,
Para haver reação de neutralização (Acido + Base -> Sal + Água), os ácidos precisam estar em forma de íons, isto é, necessitam ter sofrido ionização, ou seja, o meio reacional deverá ser aquoso. Sendo assim, a reação acontecerá na presença de água, e isso é fundamental para entendermos o que está acontecendo aqui.
Como o meio é aquoso, a amônia (NH3) também será adicionada na água, transformando-se no íon amônio, o NH4+ (amônia é uma coisa, amônio é outra coisa).
O motivo disso acontecer é devido ao par eletrônico livre do nitrogênio fazer uma ligação dativa com os íons hidrogênios presentes no meio reacional, veja:
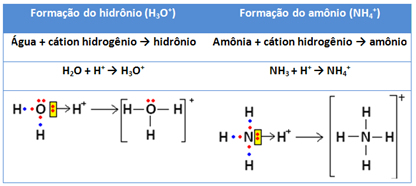
Dessa forma, toda vez que adicionar NH3 em presença de H+ livre, haverá a formação de NH4+
Assim, as reações de neutralização serão:
Primeiramente com o H2SO4, que sofre a seguinte ionização:
H2SO4 -> 2H+ + SO4-2
O ânion SO4-2 se formará o sal (NH4)2SO4, por atração eletrostática (ligação iônica):
NH4+ + SO4-2 -> (NH4)2SO4
Agora para o HNO3:
HNO3 -> H+ + NO3-
NH4+ + NO3- -> NH4NO3
Para haver reação de neutralização (Acido + Base -> Sal + Água), os ácidos precisam estar em forma de íons, isto é, necessitam ter sofrido ionização, ou seja, o meio reacional deverá ser aquoso. Sendo assim, a reação acontecerá na presença de água, e isso é fundamental para entendermos o que está acontecendo aqui.
Como o meio é aquoso, a amônia (NH3) também será adicionada na água, transformando-se no íon amônio, o NH4+ (amônia é uma coisa, amônio é outra coisa).
O motivo disso acontecer é devido ao par eletrônico livre do nitrogênio fazer uma ligação dativa com os íons hidrogênios presentes no meio reacional, veja:

Dessa forma, toda vez que adicionar NH3 em presença de H+ livre, haverá a formação de NH4+
Assim, as reações de neutralização serão:
Primeiramente com o H2SO4, que sofre a seguinte ionização:
H2SO4 -> 2H+ + SO4-2
O ânion SO4-2 se formará o sal (NH4)2SO4, por atração eletrostática (ligação iônica):
NH4+ + SO4-2 -> (NH4)2SO4
Agora para o HNO3:
HNO3 -> H+ + NO3-
NH4+ + NO3- -> NH4NO3

guipenteado- Jedi

- Mensagens : 373
Data de inscrição : 02/03/2016
Idade : 27
Localização : paranavai
 Re: Reação de Neutralização
Re: Reação de Neutralização
Caramba, que explicação boa!!!!! Obrigada por todo o cuidado e detalhamento. Entendi perfeitamente. Obrigada!!!!

dudinhamedicina2- Padawan

- Mensagens : 74
Data de inscrição : 06/06/2019
Idade : 26
Localização : Delmiro Gouveia, Alagoas, Brasil
 Tópicos semelhantes
Tópicos semelhantes» Reação de neutralização.
» Reação de Neutralização
» Reação de Neutralização
» Reação de Neutralização
» reação de neutralização
» Reação de Neutralização
» Reação de Neutralização
» Reação de Neutralização
» reação de neutralização
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













