neutralização parcial do ácido
2 participantes
Página 1 de 1
 neutralização parcial do ácido
neutralização parcial do ácido
é um exemplo de como fazer a equação de neutralização parcial do ácido, formando hidrogenossal que vi na minha apostila o exemplo é o seguinte:
ácido sulfúrico + hidróxido de sódio
o primeiro passo que foi no qual empaquei era ionizar o ácido e descobrir o ânion
no exemplo diz que o ácido sulfúrico de H2SO4 vai para HSO-4 (bissulfato)
eu não entendi essa parte pois pelo que aprendi sobre ionizar um ácido ele ficaria da seguinte forma :
SO2-4
alguém consegue me explicar porque na ionização do ácido sulfúrico temos o bissulfato é não a forma como eu apresentei ?
ácido sulfúrico + hidróxido de sódio
o primeiro passo que foi no qual empaquei era ionizar o ácido e descobrir o ânion
no exemplo diz que o ácido sulfúrico de H2SO4 vai para HSO-4 (bissulfato)
eu não entendi essa parte pois pelo que aprendi sobre ionizar um ácido ele ficaria da seguinte forma :
SO2-4
alguém consegue me explicar porque na ionização do ácido sulfúrico temos o bissulfato é não a forma como eu apresentei ?

vnlvih- Padawan

- Mensagens : 53
Data de inscrição : 29/07/2014
Idade : 29
Localização : são paulo
 Re: neutralização parcial do ácido
Re: neutralização parcial do ácido
Isso ocorre quando a quantidade de H+ e de OH- não estão em proporção.Por exemplo:
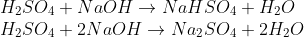
A primeira equação representa uma parcial , pois a quantidade de H+ e OH- não estão em proporção.Já a segunda , representa uma total pois a quantidade de H+ e OH- está em proporção.
A primeira equação representa uma parcial , pois a quantidade de H+ e OH- não estão em proporção.Já a segunda , representa uma total pois a quantidade de H+ e OH- está em proporção.
pedrim27- Mestre Jedi

- Mensagens : 517
Data de inscrição : 30/10/2014
Idade : 25
Localização : Minas Gerais,Brasil
 Re: neutralização parcial do ácido
Re: neutralização parcial do ácido
mas em reação de neutralização parcial existe alguma regra que diz ao se ionizar um acido só existe um H ionizavel ? pq se caisse em uma questao para forma a equação de neutralização parcial eu não conseguiria chegar ao bissulfato quando fosse ionizar o acido

vnlvih- Padawan

- Mensagens : 53
Data de inscrição : 29/07/2014
Idade : 29
Localização : são paulo
 Re: neutralização parcial do ácido
Re: neutralização parcial do ácido
Não entendi sua pergunta. Poderia refazê-la?
pedrim27- Mestre Jedi

- Mensagens : 517
Data de inscrição : 30/10/2014
Idade : 25
Localização : Minas Gerais,Brasil
 Re: neutralização parcial do ácido
Re: neutralização parcial do ácido
se levassemos em conta que eu nao teria a equação de neutralização parcial, mas o exercicio pedisse neutralização parcial, existe alguma maneira deu saber que ao ionizar o acido sufulrico eu teria o bissulfato ou esse tipo de coisa eu tenho que decorar ?

vnlvih- Padawan

- Mensagens : 53
Data de inscrição : 29/07/2014
Idade : 29
Localização : são paulo
 Re: neutralização parcial do ácido
Re: neutralização parcial do ácido
Sim ué, o ácido sulfúrico possui 2 hidrogênios ionizáveis.Para fazer ligação ele precisa de liberar no mínimo um.Então temos HSO4- ou SO4^{-2}.Parcial é HSO4- , total é SO4^{-2}.Há ácidos com mais hidrogênios ionizáveis, como,por exemplo,o H3PO4,H3PO3,mas as questões que eles aparecem , sempre há uma especificação sobre quantos hidrogênios foram liberados.
pedrim27- Mestre Jedi

- Mensagens : 517
Data de inscrição : 30/10/2014
Idade : 25
Localização : Minas Gerais,Brasil
 Tópicos semelhantes
Tópicos semelhantes» Neutralização parcial/total
» sobre reações de neutralização parcial
» sobre reações de neutralização parcial
» Neutralização de ácido
» Neutralização de ácido
» sobre reações de neutralização parcial
» sobre reações de neutralização parcial
» Neutralização de ácido
» Neutralização de ácido
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













