Questão sobre P.F., nuvem eletrônica e massa atômica.
2 participantes
Página 1 de 1
 Questão sobre P.F., nuvem eletrônica e massa atômica.
Questão sobre P.F., nuvem eletrônica e massa atômica.
Questão: Explique por que, na família dos halogênios, a temperatura de fusão aumenta com o número atômico.
P.S.- e pq tbm q, para a família 1A, é o inverso? Isso me soa muito estranho...
P.S.- e pq tbm q, para a família 1A, é o inverso? Isso me soa muito estranho...
Última edição por Ian Fáuzi em Sex 15 Set 2023, 15:33, editado 1 vez(es)

Ian Fáuzi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 22/01/2021
Idade : 21
Localização : Juiz de Fora- MG
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Ian Fáuzi, primeiro é importante você não confundir átomos da familia dos halogênios com moléculas da família dos halogênios, o que aumenta é o PF e PE das moléculas diatômicas formadas por átomos da referida família, desta forma temos:Ian Fáuzi escreveu:Questão: Explique por que, na família dos halogênios, a temperatura de fusão aumenta com o número atômico.
P.S.- e pq tbm q, para a família 1A, é o inverso? Isso me soa muito estranho...
Os Pontos de fusão e pontos de ebulição dos halogênios aumentam descendo o grupo 7. Isso ocorre porque, descendo o grupo 7:
- as moléculas ficam maiores
- as forças intermoleculares Tornar-se mais forte
- mais energia é necessário para superar essas forças
Group 7 - the halogens
The group 7 elements are all reactive non-metals. They react with metals to form metal halides, and with hydrogen to form acidic hydrogen halides. Reactivity decreases down the group.
Part ofChemistry (Single Science)Groups in the periodic table
Add to My Bitesize
TwitterFacebookWhatsAppShare
Revise
Video
Test
Physical properties of the halogens
Group 7 contains non-metal elements placed in a vertical column on the right of the periodic table. The elements in group 7 are called the halogens.
Periodic table with Group 7 in red.
Group 7 is on the right-hand side of the periodic table, next to group 0
The halogens show trends in their physical and chemical properties.
Physical properties
The halogens exist as simple molecules. Each molecule contains two halogen atoms joined by a single covalent bond. The table shows the colour and physical states of chlorine, bromine and iodine at room temperature.
| Chlorine, Cl2 | Pale green | Gas |
| Bromine, Br2 | Brown | Liquid |
| Iodine, I2 | Purple-black | Solid |
- the molecules become larger
- the intermolecular forces become stronger
- more energy is needed to overcome these forces
Example
The graph shows the melting and boiling points of the first four group 7 elements. Astatine is placed below iodine in group 7. Predict the melting and boiling points of astatine, and its state at room temperature.
Bar chart showing how the melting and boiling points of the halogens increase going down group 7
Astatine should have a melting point of about 300°C and a boiling point of about 340°C. This means that it will be solid at room temperature.
https://www.bbc.co.uk/bitesize/guides/zg337p3/revision/1

Jigsaw- Monitor

- Mensagens : 562
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
Ian Fáuzi gosta desta mensagem
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
No caso dos elementos da Familia dos metais alcalinos-terrosos estamos nos referindo a átomos, desta forma temos que: "À medida que os átomos aumentam de tamanho, a distância entre os núcleos e esses elétrons deslocalizados aumenta; portanto, as atrações caem. Os átomos são mais facilmente separados para formar um líquido e depois um gás."Ian Fáuzi escreveu:Questão: Explique por que, na família dos halogênios, a temperatura de fusão aumenta com o número atômico.
P.S.- e pq tbm q, para a família 1A, é o inverso? Isso me soa muito estranho...
Trends in melting and boiling points
mptbptchart.gif
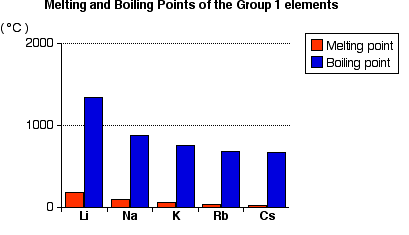
The figure above shows melting and boiling points of the Group 1 elements. Both the melting and boiling points decrease down the group.
When any of the Group 1 metals is melted, the metallic bond is weakened enough for the atoms to move more freely, and is broken completely when the boiling point is reached. The decrease in melting and boiling points reflects the decrease in the strength of each metallic bond.
The atoms in a metal are held together by the attraction of the nuclei to electrons which are delocalized over the whole metal mass. As the atoms increase in size, the distance between the nuclei and these delocalized electrons increases; therefore, attractions fall. The atoms are more easily pulled apart to form a liquid, and then a gas. As previously discussed, each atom exhibits a net pull from the nuclei of +1. The increased charge on the nucleus down the group is offset by additional levels of screening electrons. As before, the trend is determined by the distance between the nucleus and the bonding electrons.
https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Supplemental_Modules_and_Websites_(Inorganic_Chemistry)/Descriptive_Chemistry/Elements_Organized_by_Group/Group_01%3A_Hydrogen_and_the_Alkali_Metals/1Group_1%3A_Properties_of_Alkali_Metals

Jigsaw- Monitor

- Mensagens : 562
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
Ian Fáuzi gosta desta mensagem
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Acho que entendi, Jigsaw, essa diferença na tendência dos P.F. e P.E. é devida a razões diferentes. O que havia me confundido inicialmente é que, à medida que "percorro", de cima para baixo, a família dos alcalinos, maior a massa atômica, então, em tese, mais difícil seria passar as moléculas formadas para o estado líquido ou sólido. Mas, como vc bem deixou claro, estava fazendo uma confusão entre as propriedades físicas de átomos e de moléculas. Realmente faz sentido os pontos de fusão e ebulição diminuírem à medida que aumenta-se o raio atômico, já que os elétrons tendem a ficar mais externos ao núcleo, enfraquecendo as ligações metálicas, enquanto que para as moléculas do halogênio, apesar de o raio atômico aumentar, isso é benéfico, pois primeiro que o efeito de massa que eu achava que se aplicaria aos átomos de metal nesse caso é válido, segundo que as nuvens eletrônicas aumentam, favorecendo a polarização das ligações intermoleculares, o que as fortalecem.
Seria esse o raciocínio correto, então? Corrija-me por favor caso tenha falado alguma besteira.
Seria esse o raciocínio correto, então? Corrija-me por favor caso tenha falado alguma besteira.

Ian Fáuzi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 22/01/2021
Idade : 21
Localização : Juiz de Fora- MG
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Acho que entendi, Jigsaw, essa diferença na tendência dos P.F. e P.E. é devida a razões diferentes. O que havia me confundido inicialmente é que, à medida que "percorro", de cima para baixo, a família dos alcalinos, maior a massa atômica, então, em tese, mais difícil seria passar as moléculas formadas para o estado líquido ou sólido. Mas, como vc bem deixou claro, estava fazendo uma confusão entre as propriedades físicas de átomos e de moléculas. Realmente faz sentido os pontos de fusão e ebulição diminuírem à medida que aumenta-se o raio atômico, já que os elétrons tendem a ficar mais externos ao núcleo, enfraquecendo as ligações metálicas, enquanto que para as moléculas do halogênio, apesar de o raio atômico aumentar, isso é benéfico, pois primeiro que o efeito de massa que eu achava que se aplicaria aos átomos de metal nesse caso é válido, segundo que as nuvens eletrônicas aumentam, favorecendo a polarização das ligações intermoleculares, o que as fortalecem.Jigsaw escreveu:No caso dos elementos da Familia dos metais alcalinos-terrosos estamos nos referindo a átomos, desta forma temos que: "À medida que os átomos aumentam de tamanho, a distância entre os núcleos e esses elétrons deslocalizados aumenta; portanto, as atrações caem. Os átomos são mais facilmente separados para formar um líquido e depois um gás."Ian Fáuzi escreveu:Questão: Explique por que, na família dos halogênios, a temperatura de fusão aumenta com o número atômico.
P.S.- e pq tbm q, para a família 1A, é o inverso? Isso me soa muito estranho...
Trends in melting and boiling points
mptbptchart.gif
The figure above shows melting and boiling points of the Group 1 elements. Both the melting and boiling points decrease down the group.
When any of the Group 1 metals is melted, the metallic bond is weakened enough for the atoms to move more freely, and is broken completely when the boiling point is reached. The decrease in melting and boiling points reflects the decrease in the strength of each metallic bond.
The atoms in a metal are held together by the attraction of the nuclei to electrons which are delocalized over the whole metal mass. As the atoms increase in size, the distance between the nuclei and these delocalized electrons increases; therefore, attractions fall. The atoms are more easily pulled apart to form a liquid, and then a gas. As previously discussed, each atom exhibits a net pull from the nuclei of +1. The increased charge on the nucleus down the group is offset by additional levels of screening electrons. As before, the trend is determined by the distance between the nucleus and the bonding electrons.
https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Supplemental_Modules_and_Websites_(Inorganic_Chemistry)/Descriptive_Chemistry/Elements_Organized_by_Group/Group_01%3A_Hydrogen_and_the_Alkali_Metals/1Group_1%3A_Properties_of_Alkali_Metals
Seria esse o raciocínio correto, então? Corrija-me por favor caso tenha falado alguma besteira.

Ian Fáuzi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 22/01/2021
Idade : 21
Localização : Juiz de Fora- MG
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Ian Fáuzi, me parece que o seu raciocínio está correto, apenas para complementar e/ou explicar de uma outra forma, no caso dos metais alcalinos "A diminuição dos pontos de fusão e ebulição no grupo pode ser explicada pela camada adicional sendo adicionada ao elemento anterior, fazendo com que o raio atômico aumente. O aumento do raio atômico significa forças mais fracas entre os átomos e, portanto, um ponto de fusão e ebulição mais baixo"., ou seja, as forças de atração entre átomos é inversamente proporcional ao raio atômico:Ian Fáuzi escreveu:Acho que entendi, Jigsaw, essa diferença na tendência dos P.F. e P.E. é devida a razões diferentes. O que havia me confundido inicialmente é que, à medida que "percorro", de cima para baixo, a família dos alcalinos, maior a massa atômica, então, em tese, mais difícil seria passar as moléculas formadas para o estado líquido ou sólido. Mas, como vc bem deixou claro, estava fazendo uma confusão entre as propriedades físicas de átomos e de moléculas. Realmente faz sentido os pontos de fusão e ebulição diminuírem à medida que aumenta-se o raio atômico, já que os elétrons tendem a ficar mais externos ao núcleo, enfraquecendo as ligações metálicas, enquanto que para as moléculas do halogênio, apesar de o raio atômico aumentar, isso é benéfico, pois primeiro que o efeito de massa que eu achava que se aplicaria aos átomos de metal nesse caso é válido, segundo que as nuvens eletrônicas aumentam, favorecendo a polarização das ligações intermoleculares, o que as fortalecem.
Seria esse o raciocínio correto, então? Corrija-me por favor caso tenha falado alguma besteira.
Alkali Metals have lower melting and boiling Points
All Group 1 elements have one electron in their outermost shell which is held very weakly by the nucleus. This electron can drift further from the nucleus than in most atoms of other elements. This results in Group 1 elements having larger atomic radii than those elements that follow them in their respective periods. The large atomic size results in weaker forces between neighbouring atoms. It is these weaker attractive forces due to the large atomic radii between neighbouring atoms of Group 1 elements that result in lower melting and boiling points when compared to other metals.
The decrease in melting and boiling points down the group can be explained by the additional shell being added to the previous element causing the atomic radius to increase. The increasing atomic radius means weaker forces between the atoms and so a lower melting and boiling point.
http://www.passmyexams.co.uk/GCSE/chemistry/physical-properties-of-alkali-metals.html
No caso dos halogênios vale a seguinte explicação: "O ponto de ebulição dos halogênios aumenta à medida que você desce no grupo. Os halogênios existem como moléculas diatômicas, com ambos os átomos compartilhando um elétron para preencher completamente a camada externa. O aumento da ebulição (e do ponto de fusão) pode ser atribuído ao aumento das forças intermoleculares (van der Waals). O número de elétrons aumenta em cada elemento descendo no grupo, o que leva a um aumento de dipolos temporários que podem ser configurados. (nota lateral, forças de van der Waals":
Describe the trend in boiling point of the halogens.
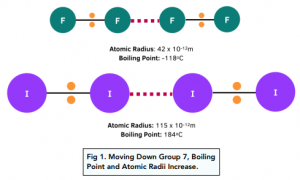
The boiling point of the halogens increases as you go down the group. The halogens exist as diatomic molecules, with both atoms sharing an electron to completely fill the outer shell. The increase in boiling (and melting point) can be attributed to the increase in intermolecular forces (van der Waals). The number of electrons increases in each element going down the group, this leads to an increase in temporary dipoles which can be set up. (side note, van der Waals forces: electrons move randomly around the nucleus of an atom, at any one time there may be more electrons on one side of a molecule creating a temporary negative charge on that side and a positive charge on the other - an instantaneous dipole. This is what holds the halogens together) In addition, the size of the molecules increases going down the group - this gives more 'space' for the electrons to sit in, this results in a reduced repulsion i.e. the electrons repel each other less. However, this is a side factor and is only particularly relevant for fluorine. This means that it is required to supply more heat in order to overcome these forces.
https://www.mytutor.co.uk/answers/26944/GCSE/Chemistry/Describe-the-trend-in-boiling-point-of-the-halogens/
Pelo que entendi a medida que ocorre aumento do raio atômico dos halogênios aumenta a probabilidade de ocorrer a polarização (deslocalização) dos eletrons, caracterizando os dipolos induzidos ou instantâneos, isso favorece as chamadas dispersões de London, mas você pode contabilizar tambem o aumento do PM para caracterizar o aumento dos PF e PE:
REFERÊNCIAS:
[1] http://www.passmyexams.co.uk/GCSE/chemistry/physical-properties-of-alkali-metals.html
[2] https://www.mytutor.co.uk/answers/26944/GCSE/Chemistry/Describe-the-trend-in-boiling-point-of-the-halogens/





Jigsaw- Monitor

- Mensagens : 562
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
Ian Fáuzi gosta desta mensagem
 Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Re: Questão sobre P.F., nuvem eletrônica e massa atômica.
Perfeito, Jigsaw, muito obrigado pelas referências e pelas colocações, que Deus te abençoe! 


Ian Fáuzi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 22/01/2021
Idade : 21
Localização : Juiz de Fora- MG
 Tópicos semelhantes
Tópicos semelhantes» dúvida sobre massa atômica
» Questão FGV - SP - Massa atômica
» Questão sobre distribuição eletronica
» Questao sobre distribuição eletrônica!
» Massa atômica, massa molecular - vunesp
» Questão FGV - SP - Massa atômica
» Questão sobre distribuição eletronica
» Questao sobre distribuição eletrônica!
» Massa atômica, massa molecular - vunesp
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













