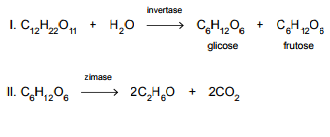UEFS Estudo dos gases+cálculo estequiométrico
+2
MalcolnMed
caiomslk
6 participantes
Página 2 de 2
Página 2 de 2 •  1, 2
1, 2
 UEFS Estudo dos gases+cálculo estequiométrico
UEFS Estudo dos gases+cálculo estequiométrico
Relembrando a primeira mensagem :
Sabendo que o volume molar de qualquer gás, nas condições ambientais de temperatura e pressão (CATP), é de 25 L ⋅ mol–1, a fermentação alcoólica de 1,0 kg de sacarose(massa molar 342 g ⋅ mol–1), em reação com rendimento de 70%, produz, nas CATP,um volume de CO2 próximo a
(A) 205 L.
(B) 170 L.
(C) 290 L.
(D) 330 L.
(E) 50 L.
- gabarito:
- A.
Feras,poderiam resolver a questão por favor ? acredito que esteja incorreta.

caiomslk- Jedi

- Mensagens : 453
Data de inscrição : 25/10/2016
Idade : 25
Localização : Feira de Santana, Bahia, Brasil
 Re: UEFS Estudo dos gases+cálculo estequiométrico
Re: UEFS Estudo dos gases+cálculo estequiométrico
Shelly ws escreveu:na verdade é 2.180 sendo que a massa da molécula de glicose é 180g mais a massa da molécula de sacarose que também vale 180g, assim sendo a massa total 2 vezes 180g.
De onde veio os 2180g
Ah sim! Não notei.
Acredito que se fosse uma questão aberta poucas pessoas iriam considerar tanto a glicose como a frutose, uma vez que a imagem só da o exemplo de uma. Eu iria rodar, rs.

AlessandroMDO- Jedi

- Mensagens : 436
Data de inscrição : 20/09/2016
Idade : 24
Localização : Ipuã - SP
 Re: UEFS Estudo dos gases+cálculo estequiométrico
Re: UEFS Estudo dos gases+cálculo estequiométrico
Correto Shelly 
Uma bela questão, Alessandro. Tem cara de ser uma questão pra 2 fase, aberta. Bom estarmos atentos xD
Uma bela questão, Alessandro. Tem cara de ser uma questão pra 2 fase, aberta. Bom estarmos atentos xD

MalcolnMed- Mestre Jedi

- Mensagens : 705
Data de inscrição : 03/04/2017
Idade : 26
Localização : São Paulo
 Re: UEFS Estudo dos gases+cálculo estequiométrico
Re: UEFS Estudo dos gases+cálculo estequiométrico
Valeu brother,sucesso no vest !!!!MalcolnMed escreveu:Fala galera! Depois de dar uma segunda olhada, percebi que o gabarito está correto. Desatenção minha xD
Segue a resolução:
1 mol de sacarose (C12H22O11) produz dois mols do monossacarideos (C6H11O6).
342g (massa molar do sacarideo) - 2.180g (MM glic/fru
1000g - x
X= 1052g aproximadamente, como o rendimento é de 70%, 736g aproximadamente.
Da fórmula:
C6H11O6 -> 2CO2
180g - 50L
736g - x litros
X= 204,44 litros
Aproximadamente 205, como dito na alternativa A.
Bela questão xD
Bons estudos!!

caiomslk- Jedi

- Mensagens : 453
Data de inscrição : 25/10/2016
Idade : 25
Localização : Feira de Santana, Bahia, Brasil
Página 2 de 2 •  1, 2
1, 2
 Tópicos semelhantes
Tópicos semelhantes» UEFS Cálculo Estequiométrico
» Cálculo Estequiométrico - (UEFS 2017.1)
» estudo dos gases uefs
» Cálculo Estequiométrico
» Cálculo Estequiométrico
» Cálculo Estequiométrico - (UEFS 2017.1)
» estudo dos gases uefs
» Cálculo Estequiométrico
» Cálculo Estequiométrico
Página 2 de 2
Permissões neste sub-fórum
Não podes responder a tópicos