Queima de combustível
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Queima de combustível
Queima de combustível
A queima de combustíveis sempre leva à liberação de quantidades consideráveis de energia. Um exemplo é a combustão do etanol, que pode ser representada por:
&space;+&space;3O_{2}(g)&space;\rightarrow&space;2CO_{2}(g)+&space;3H_{2}O(l))

Nesse sentido, é correto afirmar que:
A) 3 mols de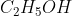 absorvem 4104 kJ de energia.
absorvem 4104 kJ de energia.
B) 3 mols de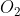 quando são consumidos na reação liberam 456 kJ de energia.
quando são consumidos na reação liberam 456 kJ de energia.
C) 23 g de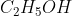 liberam 68,4 kJ de energia.
liberam 68,4 kJ de energia.
D) Quando a reação libera 1368 kJ de energia são formados 56 g de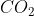 .
.
E) Para se liberar 6840 kJ de energia é necessário se queimar 5 mols de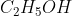 .
.
Nesse sentido, é correto afirmar que:
A) 3 mols de
B) 3 mols de
C) 23 g de
D) Quando a reação libera 1368 kJ de energia são formados 56 g de
E) Para se liberar 6840 kJ de energia é necessário se queimar 5 mols de
- Gabarito:
- E
valeriasjs- Jedi

- Mensagens : 424
Data de inscrição : 09/02/2015
Idade : 28
Localização : Aracaju - SE
 Re: Queima de combustível
Re: Queima de combustível
Pela resposta, acho que a reação tem o ∆H = –1368 kJ/mol
A) O cálculo está correto, mas ele não absorve. ∆H < 0. Reação exotérmica.
B) Segundo a reação, 3 mols liberam exatamente o ∆H, que é 1368 kJ.
C) 23 g tem meio mol. Meio mol libera 1368/2 = 684 kJ.
D) 1368 kJ são liberados quado são formados 2 mols de CO2. Dois mols de CO2 têm 88 g.
E) 1 mol ------ 1368
x mol ------ 6840
x = 5 mols
A) O cálculo está correto, mas ele não absorve. ∆H < 0. Reação exotérmica.
B) Segundo a reação, 3 mols liberam exatamente o ∆H, que é 1368 kJ.
C) 23 g tem meio mol. Meio mol libera 1368/2 = 684 kJ.
D) 1368 kJ são liberados quado são formados 2 mols de CO2. Dois mols de CO2 têm 88 g.
E) 1 mol ------ 1368
x mol ------ 6840
x = 5 mols

Gustavoadp- Estrela Dourada

- Mensagens : 1036
Data de inscrição : 05/07/2014
Idade : 26
Localização : Recife, PE
 Re: Queima de combustível
Re: Queima de combustível
Fiquei com dúvida na letra A.
A) Os reagentes não devem absorver energia para terem suas ligações quebradas e os produtos liberam quando são formados, daí então, o combustível, então, precisaria de uma energia de absorção (ignição) pra daí começar a queimar, mas quando novas ligações se formam, libera mais energia, sendo exotérmica? Não tenho confiança nessa teoria.
A) Os reagentes não devem absorver energia para terem suas ligações quebradas e os produtos liberam quando são formados, daí então, o combustível, então, precisaria de uma energia de absorção (ignição) pra daí começar a queimar, mas quando novas ligações se formam, libera mais energia, sendo exotérmica? Não tenho confiança nessa teoria.

estraveneca- Jedi

- Mensagens : 337
Data de inscrição : 08/05/2016
Idade : 30
Localização : Brasil
 Tópicos semelhantes
Tópicos semelhantes» (Covest-96) Queima de combustível
» Queima
» queima da palha de aço
» "Queima" do hidrogênio
» Queima de etano
» Queima
» queima da palha de aço
» "Queima" do hidrogênio
» Queima de etano
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













