Termoquímica
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Termoquímica
Termoquímica
(IME-87) Numa experiência realizada em uma bomba calorimétrica fora m queimados totalmente 0,6000 g de um alcano. Observou-se no termômetro do calorímetro uma variação de temperatura de 24,00 °C para 27,52 °C. O equivalente em água do calorímetro é de 2,000 kg. Em seguida, os gases da combustão foram borbulhados numa solução saturada de Ca(OH)2, formando-se um sólido branco que, depois de separado e seco, apresentou uma massa de 4,170 g. Sabendo-se que o produto de solubilidade da substância que constitui o sólido branco é tal que a precipitação é total, determine:
a) a fórmula molecular do hidrocarboneto
b) o número de moles do hidrocarboneto queimado
c) o calor molar de combustão do hidrocarboneto
d) o calor de formação do hidrocarboneto no estado gasoso, em função dos calores de formação dos produtos da combustão
e) o volume que os produtos, admitidos gasosos, ocupariam nas CNTP.
Obs: Ca= 40,1 g
Gabarito: a) C5H12
b) 8,3 x 10-3 mol
c) 844,8 kcal/mol
d) ∆Hf= 844,8 + 5∆Hf(CO2) + 6∆Hf(H2O)
e) 2 L
a) a fórmula molecular do hidrocarboneto
b) o número de moles do hidrocarboneto queimado
c) o calor molar de combustão do hidrocarboneto
d) o calor de formação do hidrocarboneto no estado gasoso, em função dos calores de formação dos produtos da combustão
e) o volume que os produtos, admitidos gasosos, ocupariam nas CNTP.
Obs: Ca= 40,1 g
Gabarito: a) C5H12
b) 8,3 x 10-3 mol
c) 844,8 kcal/mol
d) ∆Hf= 844,8 + 5∆Hf(CO2) + 6∆Hf(H2O)
e) 2 L
Ryuzinho- Iniciante
- Mensagens : 4
Data de inscrição : 16/04/2020
 Re: Termoquímica
Re: Termoquímica
Eu estava procurando uma resolução dessa questão e vi que não estava resolvida. Questão boa!
Da Combustão do alcano(Reação I):

O gás que, efetivamente, reage com o Ca(OH)2 é o CO2, que, a partir da seguinte reação(Reação II), produz um sólido branco- CaCO3:

Desse modo, como a proporção é de 1:1 entre o CaCO3 e o CO2, temos que o número de mols formado é:
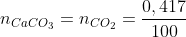
Da proporção estequiométrica da Reação I:

a)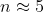
b)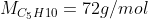
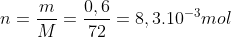
c)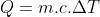
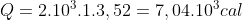
Da proporção estequiométrica(Entalpia obtida em módulo):
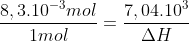
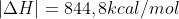
Como a reação é uma reação de combustão:
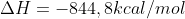
D)
Para a reação de combustão já balanceada:

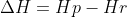

 (Valores em Kcal)
(Valores em Kcal)
E) Volume Molar=22,4 mols/L
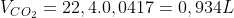
Considerando que a água é líquida na temperatura do problema:
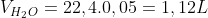
Assim, o volume total é de:

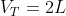
Espero ter ajudado! Grande Abraço!
Da Combustão do alcano(Reação I):
O gás que, efetivamente, reage com o Ca(OH)2 é o CO2, que, a partir da seguinte reação(Reação II), produz um sólido branco- CaCO3:
Desse modo, como a proporção é de 1:1 entre o CaCO3 e o CO2, temos que o número de mols formado é:
Da proporção estequiométrica da Reação I:
a)
b)
c)
Da proporção estequiométrica(Entalpia obtida em módulo):
Como a reação é uma reação de combustão:
D)
Para a reação de combustão já balanceada:
E) Volume Molar=22,4 mols/L
Considerando que a água é líquida na temperatura do problema:
Assim, o volume total é de:
Espero ter ajudado! Grande Abraço!

FocoNoIMEITA- Jedi

- Mensagens : 270
Data de inscrição : 05/05/2020
Idade : 21
Localização : Rio de Janeiro-RJ
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













