Equilíbrio Químico
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equilíbrio Químico
Equilíbrio Químico
Um herbicida é uma substância utilizada para controlar plantas daninhas. O glifosato [n-(fosfonometil) glicina] é um herbicida não seletivo que atua inibindo a enzima EPSP (5-enolpiruvato-chiquimato-3-fosfati sintase) responsável pela síntese de aminoácidos essenciais ao crescimento de plantas. O glifosato apresenta uma sequência de equilíbrios e constantes de dissociação de acordo com a figura abaixo.
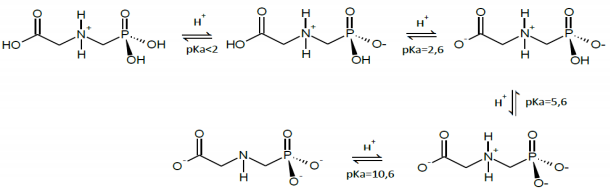
Com relação ao glifosato, seus equilíbrios e constantes de dissociação, é INcorreto afirmar:
a)O glifosato apresenta os grupos funcionais amida, carboxilato e fosfonato em sua molécula.
b)Em pH abaixo de 2,0, o glifosato apresenta carga líquida positiva.
c)Em pH acima de 11, o glifosato apresenta-se na forma trianiônica.
d)O glifosato apresenta comportamento anfótero devido aos seus grupos funcionais, podendo assumir diferentes cargas iônicas em função do pH do meio.
e)A molécula do glifosato tem a seguinte fórmula molecular: C3H8NO5P.
Estou com dificuldades em transformar pKa em pH, alguém pode me ajudar e responder a questão, mostrando o passo a passo.

Com relação ao glifosato, seus equilíbrios e constantes de dissociação, é INcorreto afirmar:
a)O glifosato apresenta os grupos funcionais amida, carboxilato e fosfonato em sua molécula.
b)Em pH abaixo de 2,0, o glifosato apresenta carga líquida positiva.
c)Em pH acima de 11, o glifosato apresenta-se na forma trianiônica.
d)O glifosato apresenta comportamento anfótero devido aos seus grupos funcionais, podendo assumir diferentes cargas iônicas em função do pH do meio.
e)A molécula do glifosato tem a seguinte fórmula molecular: C3H8NO5P.
Estou com dificuldades em transformar pKa em pH, alguém pode me ajudar e responder a questão, mostrando o passo a passo.
Última edição por Dr.Astro em Sáb 15 Jun 2019, 07:57, editado 1 vez(es)

Dr.Astro- Mestre Jedi

- Mensagens : 516
Data de inscrição : 12/06/2019
Localização : Brasil
 Re: Equilíbrio Químico
Re: Equilíbrio Químico
Dr. Astro,
Vamos tentar elucidar um pouco essa questão.
A única relação direta, que eu conheço, relacionando Ph diretamente com Pka, é a equação de equação de henderson hasselbach, utilizada nos estudos de solução tampão, e acredito que não deve ser utilizada nesse exercício pois não há dados o suficiente.
Como a questão dá apenas o Pka, não há como calcular o valor exato do Ph, apenas entender qual é a sua relação.
Quanto menor for o Pka, maior será o Ka, ou seja, maior será a força do ácido. Isto quer dizer que quanto menor for o Pka, maior será o grau de ionização do ácido e, consequentemente, menor será o Ph do meio, isto é, mais ácido será o meio. Então dá pra gente fazer uma analise de que quanto menor o Pka, menor o Ph.
Vamos as alternativas:
A) Esta alternativa já de cara é a incorreta, visto que o composto não possui amida, e sim amina
B) Em ph(neste caso, analisamos como análogo ao pka) menor que 2, o glifosato apresenta carga positiva, que veio do H+ ligado por dativa ao nitrogênio
C) Em Ph altos, a última parte da reação, o composto apresenta 3 cargas negativas
D) O glifosato é um anfótero, ou seja, tem comportamente ácido e básico. O grupo carboxila tende a liberar H+ (ácido de arrhenius), e um grupo amina (base de lewis), e apresenta cargas diferentes de acordo com o Ph do meio.
E) A molécula do glifosato em estado neutro (Primeiro, tirando a dativa do nitrogênio), apresenta a fórmula molecular que a alternativa traz
Vamos tentar elucidar um pouco essa questão.
A única relação direta, que eu conheço, relacionando Ph diretamente com Pka, é a equação de equação de henderson hasselbach, utilizada nos estudos de solução tampão, e acredito que não deve ser utilizada nesse exercício pois não há dados o suficiente.
Como a questão dá apenas o Pka, não há como calcular o valor exato do Ph, apenas entender qual é a sua relação.
Quanto menor for o Pka, maior será o Ka, ou seja, maior será a força do ácido. Isto quer dizer que quanto menor for o Pka, maior será o grau de ionização do ácido e, consequentemente, menor será o Ph do meio, isto é, mais ácido será o meio. Então dá pra gente fazer uma analise de que quanto menor o Pka, menor o Ph.
Vamos as alternativas:
A) Esta alternativa já de cara é a incorreta, visto que o composto não possui amida, e sim amina
B) Em ph(neste caso, analisamos como análogo ao pka) menor que 2, o glifosato apresenta carga positiva, que veio do H+ ligado por dativa ao nitrogênio
C) Em Ph altos, a última parte da reação, o composto apresenta 3 cargas negativas
D) O glifosato é um anfótero, ou seja, tem comportamente ácido e básico. O grupo carboxila tende a liberar H+ (ácido de arrhenius), e um grupo amina (base de lewis), e apresenta cargas diferentes de acordo com o Ph do meio.
E) A molécula do glifosato em estado neutro (Primeiro, tirando a dativa do nitrogênio), apresenta a fórmula molecular que a alternativa traz

guipenteado- Jedi

- Mensagens : 373
Data de inscrição : 02/03/2016
Idade : 27
Localização : paranavai
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico - grau de equilíbrio
» equilíbrio químico
» Equilíbrio Químico (pH)
» Equilíbrio químico.
» Equílibrio químico
» equilíbrio químico
» Equilíbrio Químico (pH)
» Equilíbrio químico.
» Equílibrio químico
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













