Meio básico
2 participantes
PiR2 :: Química :: Química Orgânica
Página 1 de 1
 Meio básico
Meio básico
(ENEM) Sabões são sais de ácidos carboxílicos de cadeia longa utilizados com a finalidade de facilitar, durante processos de lavagem, a remoção de substâncias de baixa solubilidade em água, por exemplo, óleos e gorduras. A figura a seguir representa a estrutura de uma molécula de sabão.
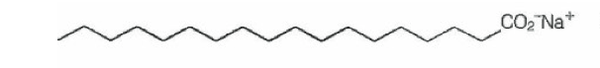
Em solução, os ânions do sabão podem hidrolisar a água e, desse modo, formar o ácido carboxílico correspondente. Por exemplo, para o estearato de sódio, é estabelecido o seguinte equilíbrio:
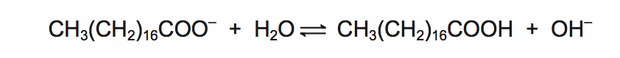
Uma vez que o ácido carboxílico formado é pouco solúvel em água e menos eficiente na remoção de gorduras, o pH do meio deve ser controlado de maneira a evitar que o equilíbrio acima seja deslocado para a direita.
Com base nas informações do texto, é correto concluir que os sabões atuam de maneira:
A) mais eficiente em pH básico.
B) mais eficiente em pH ácido.
C) mais eficiente em pH neutro.
D) eficiente em qualquer faixa de pH.
E) mais eficiente em pH ácido ou neutro.
Gabarito: A
Sempre fico confusa nesse tipo de questão. Entendo que o equilíbrio deveria ficar deslocado à esquerda, com o intuito de aumentar a eficiência na remoção gorduras. Porém, a presença do OH- na direita não caracterizaria um meio básico? No que um excesso de OH-, nesse caso, ajudaria para manter o equilíbrio à esquerda?

Em solução, os ânions do sabão podem hidrolisar a água e, desse modo, formar o ácido carboxílico correspondente. Por exemplo, para o estearato de sódio, é estabelecido o seguinte equilíbrio:
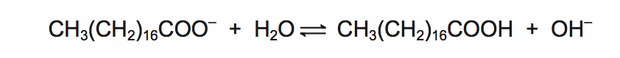
Uma vez que o ácido carboxílico formado é pouco solúvel em água e menos eficiente na remoção de gorduras, o pH do meio deve ser controlado de maneira a evitar que o equilíbrio acima seja deslocado para a direita.
Com base nas informações do texto, é correto concluir que os sabões atuam de maneira:
A) mais eficiente em pH básico.
B) mais eficiente em pH ácido.
C) mais eficiente em pH neutro.
D) eficiente em qualquer faixa de pH.
E) mais eficiente em pH ácido ou neutro.
Gabarito: A
Sempre fico confusa nesse tipo de questão. Entendo que o equilíbrio deveria ficar deslocado à esquerda, com o intuito de aumentar a eficiência na remoção gorduras. Porém, a presença do OH- na direita não caracterizaria um meio básico? No que um excesso de OH-, nesse caso, ajudaria para manter o equilíbrio à esquerda?
carolopez- Iniciante
- Mensagens : 10
Data de inscrição : 12/04/2015
Idade : 26
Localização : Niterói, Rio de Janeiro, Brasil
 Re: Meio básico
Re: Meio básico
O equilibrio é o estabelecimento de velocidades iguais de reação na "ida" e na "volta". Se você lembrar do estudo da cinética química, quanto maior a concentração de um composto, mais rápida será sua reação com outro, já que a probabilidade de que as moléculas se choquem e formem o complexo ativo aumenta.
Ora, se você aumenta a concentração de OH^(-), a reação mais rápida e fácil de ocorrer será a reação de "volta". Dessa forma, sempre haverão mais compostos no membro esquerdo do que no membro direito, já que esses últimos reagem mais rapidamente.
Ora, se você aumenta a concentração de OH^(-), a reação mais rápida e fácil de ocorrer será a reação de "volta". Dessa forma, sempre haverão mais compostos no membro esquerdo do que no membro direito, já que esses últimos reagem mais rapidamente.
 Re: Meio básico
Re: Meio básico
Muito obrigada!
carolopez- Iniciante
- Mensagens : 10
Data de inscrição : 12/04/2015
Idade : 26
Localização : Niterói, Rio de Janeiro, Brasil
 Tópicos semelhantes
Tópicos semelhantes» Balanceamento em meio básico
» balanceamento redox em meio basico
» A reação de neutralização da serotonina ocorre em meio básico.
» Derivada do quociente (básico do básico)
» Por que é meio => -1/2?
» balanceamento redox em meio basico
» A reação de neutralização da serotonina ocorre em meio básico.
» Derivada do quociente (básico do básico)
» Por que é meio => -1/2?
PiR2 :: Química :: Química Orgânica
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos













