Gases perfeitos.
5 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Gases perfeitos.
Gases perfeitos.
Um recipiente com capacidade constante de 30 L contém 1 mol de um gás considerado ideal, sob pressão P0 igual a 1,23 atm.
Considere que a massa desse gás corresponde a 4,0 g e seu calor específico, a volume constante, a 2,42 cal. g^-1. ºC^-1.
Calcule a quantidade de calor que deve ser fornecida ao gás contido no recipiente para sua pressão alcançar um valor três vezes maior do que P0.
Dados: R=0,082 atm.L/mol.K
Essa é uma questão da UERJ que discordo do gabarito oficial.
Minha resolução:
P0V=nRT0
1,23 * 30=1*0,082*T0
T0=450k
PV=nRT onde P=3P0
3(1,23)*30=1*0,082*T
T=1350K
Para a quantidade de calor, temos:
Delta T = T - T0 => Delta T =1350-450=900K
Passando delta T=900K para ºC , temos:
delta T=900-273= 627ºC
Q=m*c*delta T
Q=4*2,42*627 = 6069,36 cal
Gabarito oficial:Q = 4*2,42*900 => Q= 8,7*10³ cal
Minha dúvida ... o calor específico dado na questão é 2,42cal.g^-1.ºC^-1 e a constante universal dos gases em atm.L/mol.K ; logo teria que passar o delta T para ºC e o gabarito oficial ñ fez essa conversão ... minha resolução está errada ?
Considere que a massa desse gás corresponde a 4,0 g e seu calor específico, a volume constante, a 2,42 cal. g^-1. ºC^-1.
Calcule a quantidade de calor que deve ser fornecida ao gás contido no recipiente para sua pressão alcançar um valor três vezes maior do que P0.
Dados: R=0,082 atm.L/mol.K
Essa é uma questão da UERJ que discordo do gabarito oficial.
Minha resolução:
P0V=nRT0
1,23 * 30=1*0,082*T0
T0=450k
PV=nRT onde P=3P0
3(1,23)*30=1*0,082*T
T=1350K
Para a quantidade de calor, temos:
Delta T = T - T0 => Delta T =1350-450=900K
Passando delta T=900K para ºC , temos:
delta T=900-273= 627ºC
Q=m*c*delta T
Q=4*2,42*627 = 6069,36 cal
Gabarito oficial:Q = 4*2,42*900 => Q= 8,7*10³ cal
Minha dúvida ... o calor específico dado na questão é 2,42cal.g^-1.ºC^-1 e a constante universal dos gases em atm.L/mol.K ; logo teria que passar o delta T para ºC e o gabarito oficial ñ fez essa conversão ... minha resolução está errada ?
morenaduvida- Recebeu o sabre de luz

- Mensagens : 122
Data de inscrição : 07/09/2009
Localização : Rio de Janeiro
 Re: Gases perfeitos.
Re: Gases perfeitos.
Você está certa. Temos massa em gramas, calor específico em cal/goC, logo a temperatura deve estar em oC.
..
..
____________________________________________
In memoriam - Euclides faleceu na madrugada do dia 3 de Abril de 2018.

Lembre-se de que os vestibulares têm provas de Português também! Habitue-se a escrever corretamente em qualquer circunstância!
O Universo das coisas que eu não sei é incomensuravelmente maior do que o pacotinho de coisas que eu penso que sei.
Euclides- Fundador
- Mensagens : 32508
Data de inscrição : 07/07/2009
Idade : 74
Localização : São Paulo - SP
 Re: Gases perfeitos.
Re: Gases perfeitos.
Neste caso o valor de T-To em k ou Celsius eh igual.
Em Kelvin temos 1350-450=900
Em celsius temos 1077-177=900
Logo a diferença entre as temperaturas eh a mesma nas duas unidades.
Em Kelvin temos 1350-450=900
Em celsius temos 1077-177=900
Logo a diferença entre as temperaturas eh a mesma nas duas unidades.
thais rezende xavier- Iniciante
- Mensagens : 2
Data de inscrição : 16/11/2012
Idade : 36
Localização : iguaba, RJ, Brasil
 Re: Gases perfeitos.
Re: Gases perfeitos.
Sua resolução está errada sim ... O cálculo de ∆T será igual para os dois. Veja:
Em kelvin:
∆T = TF - TI
Em graus celcius:
∆T= (TF - 273) - (TI - 273) = TF - TI
Em kelvin:
∆T = TF - TI
Em graus celcius:
∆T= (TF - 273) - (TI - 273) = TF - TI

Leonardo Sueiro- Fera

- Mensagens : 3220
Data de inscrição : 28/06/2012
Idade : 31
Localização : Santos
 Re: Gases perfeitos.
Re: Gases perfeitos.
Está errada, como disse o leosueiro123.
Sabemos que:

E você sabe que essa "fórmula" nada mais é que uma regra de três de distâncias entre temperaturas. Perceba: uma temperatura C menos o ponto de fusão da água dividido pelo ponto de ebulição da água menos o ponto de fusão, agora para Fahrenheit e Kelvin a mesma coisa.
Então podemos fazer distâncias entre temperaturas, também. Vamos denominar temperaturas C1 e C2 para a escala Celsius e coincidentes K1 e K2 para a Kelvin. Agora vamos aplicar as distâncias, vamos supor C2>C1. Logo temos:
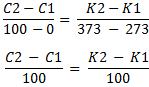
Logo: C2 - C1 = K2 - K1
Então variações de temperatura na escala Celsius tem o mesmo valor.
Como a fórmula do calor sensível é:
Q = m.c.∆T
Temos uma variação de temperatura que vale a mesma tanto para Celsius quanto para Kelvin.
Sabemos que:

E você sabe que essa "fórmula" nada mais é que uma regra de três de distâncias entre temperaturas. Perceba: uma temperatura C menos o ponto de fusão da água dividido pelo ponto de ebulição da água menos o ponto de fusão, agora para Fahrenheit e Kelvin a mesma coisa.
Então podemos fazer distâncias entre temperaturas, também. Vamos denominar temperaturas C1 e C2 para a escala Celsius e coincidentes K1 e K2 para a Kelvin. Agora vamos aplicar as distâncias, vamos supor C2>C1. Logo temos:
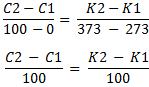
Logo: C2 - C1 = K2 - K1
Então variações de temperatura na escala Celsius tem o mesmo valor.
Como a fórmula do calor sensível é:
Q = m.c.∆T
Temos uma variação de temperatura que vale a mesma tanto para Celsius quanto para Kelvin.

Exp4nsion- Iniciante
- Mensagens : 31
Data de inscrição : 26/08/2011
Idade : 33
Localização : Petrolina, Pernambuco.
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













