Questão de estequiometria
2 participantes
Página 1 de 1
 Questão de estequiometria
Questão de estequiometria
Num recipiente foram misturados 2,0g de hidrogênio gasoso e 6,4g de oxigênio gasoso em condições de formar as substâncias água e água oxigenada. Sabendo-se que a massa de água formada é igual a 3,6g. A opção que apresenta, aproximadamente, o percentual de água oxigenada obtida ao final de todas as reações no recipiente é:
A) 10%
B) 38%
C) 41%
D) 70%
E) 80%
Gabarito: C
A) 10%
B) 38%
C) 41%
D) 70%
E) 80%
Gabarito: C
Última edição por Joaquim59 em Qua 20 Jul 2022, 09:19, editado 1 vez(es)
Joaquim59- Iniciante
- Mensagens : 5
Data de inscrição : 14/05/2021
Localização : Cruz das Almas, Bahia, Brasil
 Re: Questão de estequiometria
Re: Questão de estequiometria
Boa noite, Joaquim!
Vamos montar as duas reações:

Sabemos que foram formados 3,6 g de água, ou seja: 3,6/18 = 0,2 mol de água.
Para que tenham sido formados 0,2 mol de água, foram necessário 0,2 mol(0,4 g) de H2 e 0,1 mol(3,2 g) de O2. Para observar isso, basta seguir a estequiometria das reações.
Assim, sabemos que foram usados 0,4 g dos 2 g de hidrogênio disponíveis no recipiente e 3,2 g dos 6,4 g de oxigênio no recipiente.
O que sobra para reagir formando água oxigenada:
- 1,6 g de Hidrogênio - 0,8 mol de H2;
- 3,2 g de Oxigênio - 0,1 mol de O2;
Pela estequiometria da eq. 2, sabemos que o oxigênio será o limitante. Dessa forma, 0,1 mol de H2 reagem com 0,1 mol de O2 e produzem 0,1 mol de H2O2.
0,1 mol de H2O2 são 3,4 g.
A massa da mistura ao início é 8,4 g, a qual mantém-se ao final da reação devido à conservação das massas. Dessa forma:
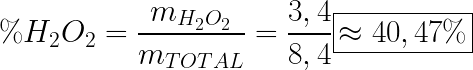
Caso você não tenha entendido algum dos passos da resolução, só mandar!
Vamos montar as duas reações:
Sabemos que foram formados 3,6 g de água, ou seja: 3,6/18 = 0,2 mol de água.
Para que tenham sido formados 0,2 mol de água, foram necessário 0,2 mol(0,4 g) de H2 e 0,1 mol(3,2 g) de O2. Para observar isso, basta seguir a estequiometria das reações.
Assim, sabemos que foram usados 0,4 g dos 2 g de hidrogênio disponíveis no recipiente e 3,2 g dos 6,4 g de oxigênio no recipiente.
O que sobra para reagir formando água oxigenada:
- 1,6 g de Hidrogênio - 0,8 mol de H2;
- 3,2 g de Oxigênio - 0,1 mol de O2;
Pela estequiometria da eq. 2, sabemos que o oxigênio será o limitante. Dessa forma, 0,1 mol de H2 reagem com 0,1 mol de O2 e produzem 0,1 mol de H2O2.
0,1 mol de H2O2 são 3,4 g.
A massa da mistura ao início é 8,4 g, a qual mantém-se ao final da reação devido à conservação das massas. Dessa forma:
Caso você não tenha entendido algum dos passos da resolução, só mandar!

Arlindocampos07- Mestre Jedi

- Mensagens : 506
Data de inscrição : 22/02/2022
Idade : 20
Localização : Cajazeiras, Paraíba, Brasil
Joaquim59 gosta desta mensagem
 Re: Questão de estequiometria
Re: Questão de estequiometria
Entendi perfeitamente, muito obrigado pela clareza! 
Joaquim59- Iniciante
- Mensagens : 5
Data de inscrição : 14/05/2021
Localização : Cruz das Almas, Bahia, Brasil
Arlindocampos07 gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» questao estequiometria
» questao estequiometria
» Questão de estequiometria
» questao estequiometria
» Questão de estequiometria
» questao estequiometria
» Questão de estequiometria
» questao estequiometria
» Questão de estequiometria
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













