Termodinâmica
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Termodinâmica
Termodinâmica
Tendo os seguintes dados para um mol de gás ideal, a T=323K, pressão inicial de 15,0 atm, pressão final de 5,0 atm, volume inicial de 10,0L e volume final de 30,0 L, esquematize em um mesmo diagrama :
a) o caminho para uma expansão reversível isotérmica;
b) o caminho, em um primeiro passo, no qual o gás é resfriado a volume constante até Pf = 5,0atm; e em um segundo passo, o gás é aquecido e expandido contra uma Pf=5,0 atm até o Vf=30,0L
c) qual a relação entre q e w?
d) em qual caminho é realizado um w maior?
Infelizmente não possuo o gabarito.
a) o caminho para uma expansão reversível isotérmica;
b) o caminho, em um primeiro passo, no qual o gás é resfriado a volume constante até Pf = 5,0atm; e em um segundo passo, o gás é aquecido e expandido contra uma Pf=5,0 atm até o Vf=30,0L
c) qual a relação entre q e w?
d) em qual caminho é realizado um w maior?
Infelizmente não possuo o gabarito.

Renan Novaes- Padawan

- Mensagens : 72
Data de inscrição : 24/12/2016
Idade : 24
Localização : São Paulo
 Re: Termodinâmica
Re: Termodinâmica
Não sei se está tudo correto, mas vamos lá...
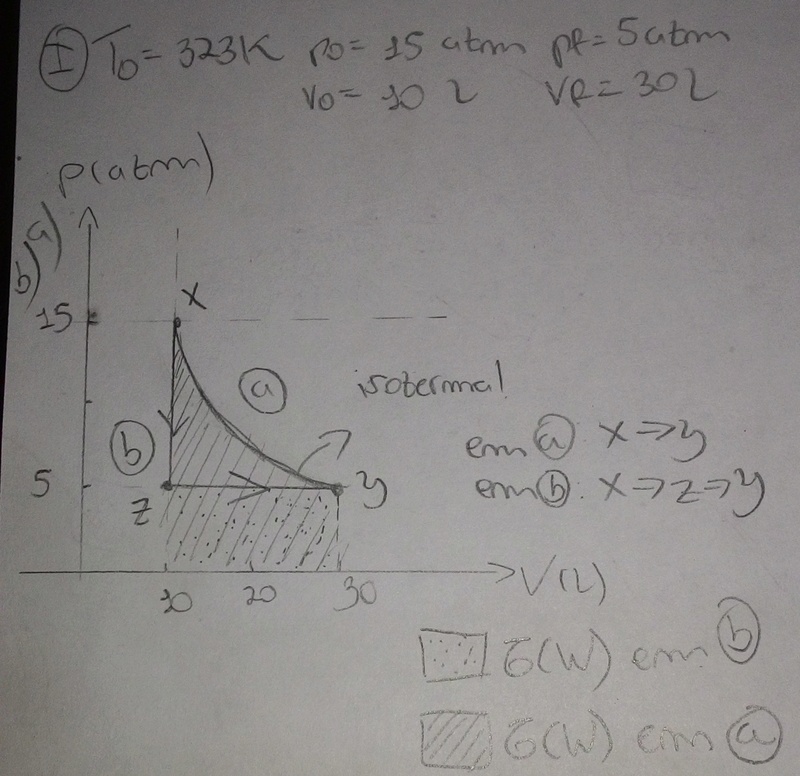
a) Esquematizei na figura. Toda isoterma é uma curva hiperbólica naquele formato, e ela tem sentido do ponto X -> ponto Y, pois ele diz que é uma expansão.
b) Esquematizei na figura. Abaixamento de pressão isocórico e expansão isobárica. Segue o caminho ponto X -> ponto Z -> ponto Y.
c) Pela primeira lei da termodinâmica:
Q = W + deltaU
Na expansão isotérmica, deltaU = 0 então Q = W
No outro caminho:
PxVx/Tx = PyVy/Ty ->
15.10/323=5.30/x, x = temperatura em Y
Resolvendo a equação, têm-se x = Ty = 323K, que é = Tx, logo, deltaU também é 0 e também vale a relação Q = W
d) O maior W é aquele cuja área do gráfico é maior. Pelo meu esquema, você pode ver que a área da expansão isotérmica é maior que a transformação em 2 etapas. Enquanto a primeira forma um retângulo e mais a área delimitada pela hipérbole (área riscada), a última forma apenas o mesmo retângulo (área pontilhada), visto que numa transformação isocórica, deltaV = 0 e portanto W=0
Acredito que seja isso, caso haja dúvidas pergunte para algum professor...

a) Esquematizei na figura. Toda isoterma é uma curva hiperbólica naquele formato, e ela tem sentido do ponto X -> ponto Y, pois ele diz que é uma expansão.
b) Esquematizei na figura. Abaixamento de pressão isocórico e expansão isobárica. Segue o caminho ponto X -> ponto Z -> ponto Y.
c) Pela primeira lei da termodinâmica:
Q = W + deltaU
Na expansão isotérmica, deltaU = 0 então Q = W
No outro caminho:
PxVx/Tx = PyVy/Ty ->
15.10/323=5.30/x, x = temperatura em Y
Resolvendo a equação, têm-se x = Ty = 323K, que é = Tx, logo, deltaU também é 0 e também vale a relação Q = W
d) O maior W é aquele cuja área do gráfico é maior. Pelo meu esquema, você pode ver que a área da expansão isotérmica é maior que a transformação em 2 etapas. Enquanto a primeira forma um retângulo e mais a área delimitada pela hipérbole (área riscada), a última forma apenas o mesmo retângulo (área pontilhada), visto que numa transformação isocórica, deltaV = 0 e portanto W=0
Acredito que seja isso, caso haja dúvidas pergunte para algum professor...
murilo_caetano- Recebeu o sabre de luz

- Mensagens : 125
Data de inscrição : 16/04/2017
Idade : 24
Localização : Bertioga, São Paulo, Brasil
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













