Reatividade de metais
3 participantes
Página 1 de 1
 Reatividade de metais
Reatividade de metais
(Fei) Têm-se 4 tubos de ensaio contendo, respectivamente, soluções com íons dos seguintes metais: AØ, Cu, Mg e Zn. Uma amostra de um destes metais é dividida em 4 partes e colocada nos tubos de ensaio citados. Observou-se reação com precipitação de metal em 3 tubos de ensaio. A amostra escolhida é do metal:
a)Al b)Mg c)Zn d)Cu e)não dá para determinar
Obs.: Já encontrei essa questão com os potenciais de redução de cada metal, no entanto, nos meus materiais de estudo, ela se apresenta numa parte de reatividade dos metais. Então gostaria de saber, analisando a fila de reatividade, como chegar à mesma resposta.
Obrigada.
Gabarito: B
a)Al b)Mg c)Zn d)Cu e)não dá para determinar
Obs.: Já encontrei essa questão com os potenciais de redução de cada metal, no entanto, nos meus materiais de estudo, ela se apresenta numa parte de reatividade dos metais. Então gostaria de saber, analisando a fila de reatividade, como chegar à mesma resposta.
Obrigada.
Gabarito: B
AnaLuC- Iniciante
- Mensagens : 15
Data de inscrição : 01/04/2013
Idade : 28
Localização : JF - MG, Brasil
 Re: Reatividade de metais
Re: Reatividade de metais
Fila de reatividade (dos elementos que eu decorei até agora):
Li K Ba Ca Na Mg Al Zn Fe Cu Hg Ag Au
Essa fila corresponde à eletropositividade decrescente dos elementos metálicos: o Li é muito mais eletropositivo que o Au, e, portanto, tem maior probabilidade de perder elétrons.
Quando o Mg é posto em uma solução com Cu(OH)2, por exemplo, ele retira o Cu e se torna Mg(OH)2, por ser mais eletropositivo.
Nenhum outro elemento poderia ser o gabarito pois não reagiriam com elementos que possuem maior eletropositividade que si mesmo. Exemplo:
Cu + Zn^(2+)
Essa reação não ocorre pois o Cu é menos eletropositivo que o Zn.
As reações que ocorrem são, portanto:
Mg + Zn^(2+) -> Mg^(2+) + Zn
Mg + Cu^(2+) -> Mg^(2+) + Cu
Mg + Al^(1+) -> Mg^(1+) + Al
A reação que não ocorre, claro:
Mg + Mg^(2+)
Cabe ressaltar que a amostra de Mg é elementar pois o enunciado afirma que é pega uma nova amostra de um dos metais (uma amostra elementar, não-aquosa, e não a amostra do tubo de ensaio).
Li K Ba Ca Na Mg Al Zn Fe Cu Hg Ag Au
Essa fila corresponde à eletropositividade decrescente dos elementos metálicos: o Li é muito mais eletropositivo que o Au, e, portanto, tem maior probabilidade de perder elétrons.
Quando o Mg é posto em uma solução com Cu(OH)2, por exemplo, ele retira o Cu e se torna Mg(OH)2, por ser mais eletropositivo.
Nenhum outro elemento poderia ser o gabarito pois não reagiriam com elementos que possuem maior eletropositividade que si mesmo. Exemplo:
Cu + Zn^(2+)
Essa reação não ocorre pois o Cu é menos eletropositivo que o Zn.
As reações que ocorrem são, portanto:
Mg + Zn^(2+) -> Mg^(2+) + Zn
Mg + Cu^(2+) -> Mg^(2+) + Cu
Mg + Al^(1+) -> Mg^(1+) + Al
A reação que não ocorre, claro:
Mg + Mg^(2+)
Cabe ressaltar que a amostra de Mg é elementar pois o enunciado afirma que é pega uma nova amostra de um dos metais (uma amostra elementar, não-aquosa, e não a amostra do tubo de ensaio).
Última edição por Christian M. Martins em Dom 28 Jun 2015, 13:56, editado 5 vez(es)
 Re: Reatividade de metais
Re: Reatividade de metais
A ordem decrescente da reatividade dos metais é a seguinte:
K>Ba>Ca>Na>Mg>Al>Zn>Fe>H>Cu>Hg>Ag>Pt>Au
Tem-se que todos os íons metálicos estão em solução, pressupõe-se, então, que estejam misturados com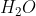 :
:




Analisando as amostras e a fila de reatividade, percebe-se que o único metál capaz de deslocar outros 3, dentre os citados, e formar um novo precipitado é o Mg. Observe:



Observação: Eu não soube fazer o simbolo de precipitado
K>Ba>Ca>Na>Mg>Al>Zn>Fe>H>Cu>Hg>Ag>Pt>Au
Tem-se que todos os íons metálicos estão em solução, pressupõe-se, então, que estejam misturados com
Analisando as amostras e a fila de reatividade, percebe-se que o único metál capaz de deslocar outros 3, dentre os citados, e formar um novo precipitado é o Mg. Observe:
Observação: Eu não soube fazer o simbolo de precipitado

Rexory- Iniciante
- Mensagens : 40
Data de inscrição : 14/01/2014
Idade : 28
Localização : Cariacica, Espírito Santo - Brasil
 Re: Reatividade de metais
Re: Reatividade de metais
Consegui entender agora, mto obrigada pelas respostas 
AnaLuC- Iniciante
- Mensagens : 15
Data de inscrição : 01/04/2013
Idade : 28
Localização : JF - MG, Brasil
 Tópicos semelhantes
Tópicos semelhantes» Reatividade dos Metais
» questão sobre a reatividade dos metais
» Reatividade !!
» reatividade
» reatividade
» questão sobre a reatividade dos metais
» Reatividade !!
» reatividade
» reatividade
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos













