Solubilidade de sais orgânicos.
2 participantes
PiR2 :: Química :: Química Orgânica
Página 1 de 1
 Solubilidade de sais orgânicos.
Solubilidade de sais orgânicos.
Julgue a seguinte alternativa:
O oxalato de cálcio é um sal solúvel em meio aquoso
Bom, pesquisando na internet, achei o seguinte:
O oxalato de cálcio é praticamente insolúvel em água.
Mesmo existindo a regra dos semelhantes, todos sabem que os sais são compostos polares, pois são iônicos. Mas todos também devem saber que existem sais solúveis e sais insolúveis. No caso dos sais insolúveis, o que determina a solubilidade é o tamanho do cátion e do ânion. Quando o cátion e o ânion tem tamanhos (raios) parecidos, as moléculas de água tem facilidade para chegar até um e outro, e consegue hidratar os íons e separá-los facilmente, o que faz com que sejam solúveis. Quando ou o cátion é muito pequeno e o ânion é muito grande (como é o caso do oxalato de cálcio, que tem um ânion enorme - o oxalato - e um cátion bem pequenininho - o cálcio), o ânion acaba por envolver o cátion e dificulta a aproximação das moléculas de água até ele, e a hidratação não é suficiente para romper a ligação entre os íons, tornando o sal insolúvel.
Gostaria de saber se essa regra funciona para determinar a solubilidade dos sais orgânicos.
O oxalato de cálcio é um sal solúvel em meio aquoso
- RESPOSTA:
- Falsa
Bom, pesquisando na internet, achei o seguinte:
O oxalato de cálcio é praticamente insolúvel em água.
Mesmo existindo a regra dos semelhantes, todos sabem que os sais são compostos polares, pois são iônicos. Mas todos também devem saber que existem sais solúveis e sais insolúveis. No caso dos sais insolúveis, o que determina a solubilidade é o tamanho do cátion e do ânion. Quando o cátion e o ânion tem tamanhos (raios) parecidos, as moléculas de água tem facilidade para chegar até um e outro, e consegue hidratar os íons e separá-los facilmente, o que faz com que sejam solúveis. Quando ou o cátion é muito pequeno e o ânion é muito grande (como é o caso do oxalato de cálcio, que tem um ânion enorme - o oxalato - e um cátion bem pequenininho - o cálcio), o ânion acaba por envolver o cátion e dificulta a aproximação das moléculas de água até ele, e a hidratação não é suficiente para romper a ligação entre os íons, tornando o sal insolúvel.
Gostaria de saber se essa regra funciona para determinar a solubilidade dos sais orgânicos.
 Re: Solubilidade de sais orgânicos.
Re: Solubilidade de sais orgânicos.
A estrutura de um sal orgânico é algo semelhante a figura abaixo:
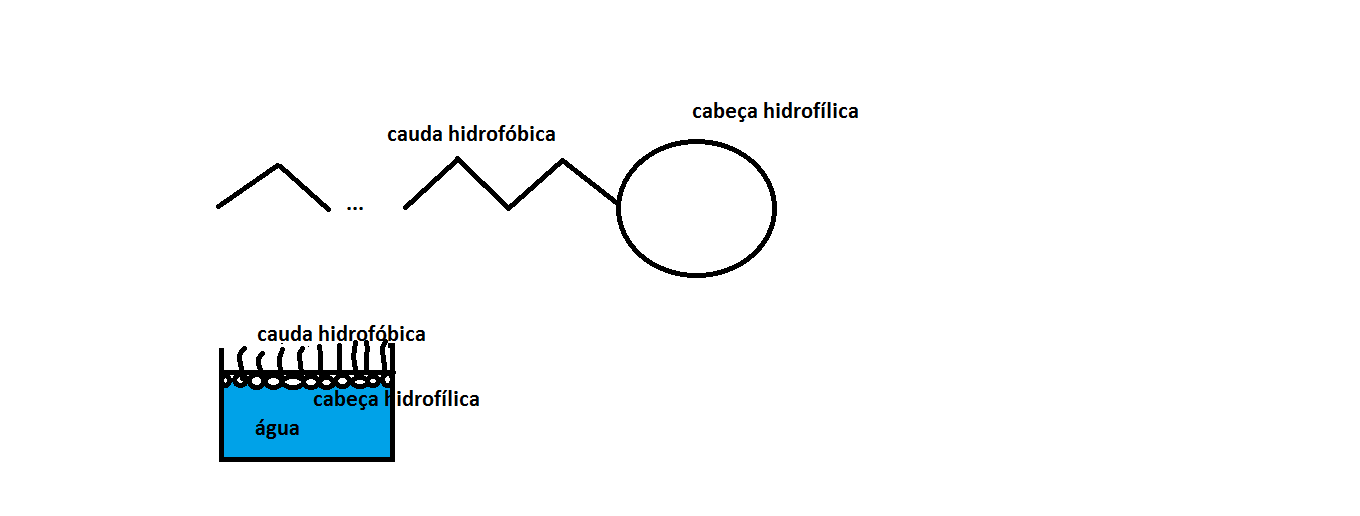
Observe que, na figura, a cabeça hidrofílica (polar) fica em contato com a água, ao passo que a cauda hidrofóbica (apolar) fica fora da água, formando uma película.
Uma boa regra prática seria dizer que os sais orgânicos são solúveis para caudas hidrofóbicas de até 3 C's.

Observe que, na figura, a cabeça hidrofílica (polar) fica em contato com a água, ao passo que a cauda hidrofóbica (apolar) fica fora da água, formando uma película.
Uma boa regra prática seria dizer que os sais orgânicos são solúveis para caudas hidrofóbicas de até 3 C's.
![JOAO [ITA]](https://2img.net/u/2713/85/25/58/avatars/20221-80.jpg)
JOAO [ITA]- Fera

- Mensagens : 866
Data de inscrição : 25/02/2012
Idade : 26
Localização : São José dos Campos,SP,Brasil
 Tópicos semelhantes
Tópicos semelhantes» Sais orgânicos
» Solubilidade de sais
» Solubilidade dos sais
» (UFMG) Solubilidade Compostos Orgânicos
» Solubilidade de orgânicos e inorgânicos
» Solubilidade de sais
» Solubilidade dos sais
» (UFMG) Solubilidade Compostos Orgânicos
» Solubilidade de orgânicos e inorgânicos
PiR2 :: Química :: Química Orgânica
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














