Termoninâmica
4 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Termoninâmica
Termoninâmica
O gráfico representa a transformação de um gás ideal que passa do estado I para o estado II e, depois, do estado II para o estado III.
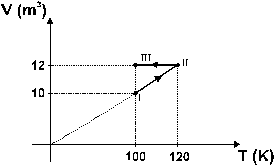
Para que o gás passe do estado I para o II, é necessário que se lhe forneçam 100 kJ de calor; para que passe do estado II para o III, que se lhe retirem 50 kJ de calor. Sabe-se que a pressão do gás no estado I é de 100 kPa. Pode-se afirmar que a variação da energia interna do gás ao passar do estado I para o III é igual a:
(A) zero
(B) - 200 kJ
(C) - 50 kJ
(D) - 140 kJ
(E) - 150 kJ

Para que o gás passe do estado I para o II, é necessário que se lhe forneçam 100 kJ de calor; para que passe do estado II para o III, que se lhe retirem 50 kJ de calor. Sabe-se que a pressão do gás no estado I é de 100 kPa. Pode-se afirmar que a variação da energia interna do gás ao passar do estado I para o III é igual a:
(A) zero
(B) - 200 kJ
(C) - 50 kJ
(D) - 140 kJ
(E) - 150 kJ
thaisreis- Iniciante
- Mensagens : 7
Data de inscrição : 13/05/2012
Idade : 28
Localização : São Luís Ma Brasil
 Re: Termoninâmica
Re: Termoninâmica
A variação de energia interna é a diferença entre o calor e o trabalho realizado pelo gás.
Matematicamente :
∆U = Q - Շ
De I a II ,perceb-se que a presão não varia , veja :
P1. V1 / T1 = P2 . V2/ T2
P1 . 10 / 100 = P2 . 12 / 120
P1 = P2
Portanto , o trabalho realizado será :
Շ = p.∆V = 100.10³.(12-10) = 200.10³J
Das variações de energia interna :
∆U(I-II) = 100.10³ - 200.10³ = -100.10³J
.'. UI - UII = -100.10³J
Como de II á III o volume não varia , o gás não realiza trabalho , visto que : Շ = p.∆V
Como ∆V = 0 -> Շ = 0
Consequencia :
∆U = Q - Շ ->
∆U = Q
Como foi retirado 50kJ
Temos que UII - UIII = -50kJ
Somando a primeira equação com a primeira , veja o que acontece :
UI - UII = -100.10³J
UII - UIII = -50.10³J
UI - UIII = -150.10³J = -150kJ
Gabarito : Letra (E)
Matematicamente :
∆U = Q - Շ
De I a II ,perceb-se que a presão não varia , veja :
P1. V1 / T1 = P2 . V2/ T2
P1 . 10 / 100 = P2 . 12 / 120
P1 = P2
Portanto , o trabalho realizado será :
Շ = p.∆V = 100.10³.(12-10) = 200.10³J
Das variações de energia interna :
∆U(I-II) = 100.10³ - 200.10³ = -100.10³J
.'. UI - UII = -100.10³J
Como de II á III o volume não varia , o gás não realiza trabalho , visto que : Շ = p.∆V
Como ∆V = 0 -> Շ = 0
Consequencia :
∆U = Q - Շ ->
∆U = Q
Como foi retirado 50kJ
Temos que UII - UIII = -50kJ
Somando a primeira equação com a primeira , veja o que acontece :
UI - UII = -100.10³J
UII - UIII = -50.10³J
UI - UIII = -150.10³J = -150kJ
Gabarito : Letra (E)
 Re: Termoninâmica
Re: Termoninâmica
De imediato, também havia encontrado a resposta -150kJ (que é o gabarito oficial).Mas me deparei com outra opção de resposta: se no processo (ao passar do estado I para o III) ∆T=0, então ∆U=0.
Seria essa constatação correta? A resposta ∆U=0 seria válida?
Seria essa constatação correta? A resposta ∆U=0 seria válida?
Última edição por Simone 1000 em Dom 22 Jul 2012, 20:59, editado 1 vez(es)
Simone 1000- Iniciante
- Mensagens : 5
Data de inscrição : 22/07/2012
Idade : 60
Localização : Vitória, Espírito Santo, Brasil
 Re: Termoninâmica
Re: Termoninâmica
Simone 1000 escreveu:Também havia encontrado a resposta -150kJ (que é o gabarito oficial).
Mas me deparei com uma questão: se no processo global (ao passar do estado I para o III) ∆T=0, então ∆U=0.
Seria essa constatação correta?
Sim, está correta.
A variação de energia interna só depende da temperatura.
Se não houver variação de temperatura, não há variação da energia interna.
 Problema
Problema
Parece-me que há um problema com essa questão. Numa expansão isobárica, a quantidade de calor (Q) absorvida pelo gás é sempre maior que o trabalho realizado. De acordo com o enunciado, o gás recebe 100kJ e realiza trabalho de 200KJ? Acho que essa questão deveria ter sido anulada.
h.dreite- Iniciante
- Mensagens : 1
Data de inscrição : 31/08/2017
Idade : 46
Localização : Mesquita
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














