eletroquimica
2 participantes
Página 1 de 1
 eletroquimica
eletroquimica
Uma soluçao de cloreto de prata é eletrolizada durante 965s por uma corrente elétrica de 1A. Qual a massa de prata depositada no cátodo?
Dado: Ag = 108g/mol
Dado: Ag = 108g/mol
9090help- Padawan

- Mensagens : 70
Data de inscrição : 10/02/2013
Idade : 28
Localização : uberlandia
 Re: eletroquimica
Re: eletroquimica
Essa questão não é difícil. Acho que faltou dá a constante, mas independente disso:
Constante de Faraday = 96.500 C/mol
Reação catódica: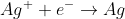
Calculando a carga fornecida: Q = i.∆t --> Q = 1A.965 s = 965 C
1 mol e ------ 1 mol Ag
96.500 C ---- 108 g Ag
965 C ------- m
m = 1,08 g de Ag
--> Acho que basta só você dá uma revisada na leitura de seu livro. Esse tipo de questão se repete muito.
Constante de Faraday = 96.500 C/mol
Reação catódica:
Calculando a carga fornecida: Q = i.∆t --> Q = 1A.965 s = 965 C
1 mol e ------ 1 mol Ag
96.500 C ---- 108 g Ag
965 C ------- m
m = 1,08 g de Ag
--> Acho que basta só você dá uma revisada na leitura de seu livro. Esse tipo de questão se repete muito.

schow- Jedi

- Mensagens : 446
Data de inscrição : 03/01/2013
Idade : 28
Localização : Fortaleza-CE
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













