Termologia
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Termologia
Termologia
Em um calorímetro ideal, colocam-se as massas "Mv"
de vapor de água a 100 °C e "Mg" de gelo a 0 °C, sob pressão
normal. O gráfico mostra como variaram as temperaturas
dessas massas em função das quantidades de calor trocadas:

Sendo o calor latente de fusão do gelo 80 cal/g, o de vaporiza-
ção da água 540 cal/g e o calor específico de água 1 cal/g °C,
determine:
a) a massa Mv
b) a massa Mg
c) a temperatura θ de equilíbrio térmico.
de vapor de água a 100 °C e "Mg" de gelo a 0 °C, sob pressão
normal. O gráfico mostra como variaram as temperaturas
dessas massas em função das quantidades de calor trocadas:
Sendo o calor latente de fusão do gelo 80 cal/g, o de vaporiza-
ção da água 540 cal/g e o calor específico de água 1 cal/g °C,
determine:
a) a massa Mv
b) a massa Mg
c) a temperatura θ de equilíbrio térmico.
- Gabarito:
- a) 10g b) 50g c) 40°C
- Dúvida:
- Saiu tranquilamente, fiz usando o gráfico considerando apenas o aquecimento da água que veio do gelo. Tenho a seguinte dúvida: E a água que condensou ? por quê usando apenas a água que veio do derretimento do gelo dá gabarito ?
Última edição por Reverse. em Seg 04 Out 2021, 20:40, editado 1 vez(es)

Reverse.- Jedi

- Mensagens : 341
Data de inscrição : 05/06/2021
 Re: Termologia
Re: Termologia
Olá Reverse;
Não entendi muito bem sua dúvida, vou resolver parte por parte, se não entender alguma passagem só falar!
a) O vapor de água à 100 °C cede 5400 calorias para o gelo, logo:
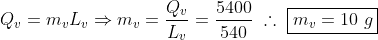
b) O gelo à 0°C absorve 4000 calorias para sua transformação completa do estado sólido para o líquido, portanto:
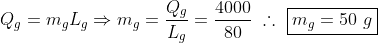
c) Existem algumas maneiras para calcular a temperatura final, utilizar do princípio conservativo e calcular todas as energias que atuam no sistema, ou pegar partes específicas, veja:
Depois que o gelo se transforma totalmente em líquido, temos mais 2000 calorias absorvidas pelo mesmo, temos:
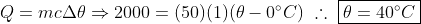
Ainda poderíamos ter partido do pressuposto que depois que o vapor de água se transforma totalmente em água líquida, em seguida, ele cede mais 600 calorias para chegar à temperatura de equilíbrio:
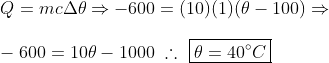
Não importa qual método você escolher, basta ser fiel a um deles e seguir até o final, trata-se de conservação da energia total. Espero que tenha ficado claro!
Não entendi muito bem sua dúvida, vou resolver parte por parte, se não entender alguma passagem só falar!
a) O vapor de água à 100 °C cede 5400 calorias para o gelo, logo:
b) O gelo à 0°C absorve 4000 calorias para sua transformação completa do estado sólido para o líquido, portanto:
c) Existem algumas maneiras para calcular a temperatura final, utilizar do princípio conservativo e calcular todas as energias que atuam no sistema, ou pegar partes específicas, veja:
Depois que o gelo se transforma totalmente em líquido, temos mais 2000 calorias absorvidas pelo mesmo, temos:
Ainda poderíamos ter partido do pressuposto que depois que o vapor de água se transforma totalmente em água líquida, em seguida, ele cede mais 600 calorias para chegar à temperatura de equilíbrio:
Não importa qual método você escolher, basta ser fiel a um deles e seguir até o final, trata-se de conservação da energia total. Espero que tenha ficado claro!

qedpetrich- Monitor

- Mensagens : 2496
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
Reverse. gosta desta mensagem
 Re: Termologia
Re: Termologia
Percebi que errei uma mísera soma em uma das tentativas ( usei o vapor de água liquefeito quando errei) e tentei justificar com algo totalmente desconexo kkkk, maldita falta de atenção. Obrigado, meu bom.

Reverse.- Jedi

- Mensagens : 341
Data de inscrição : 05/06/2021
qedpetrich gosta desta mensagem
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














