equilíbrio químico
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 equilíbrio químico
equilíbrio químico
Uma reação exotérmica, representada por ❍ (g) ⇄ ● (g), foi acompanhada até o equilíbrio químico, como representado no sistema X

Algumas alterações foram realizadas, separada e individualmente, no sistema X.
Alteração 1 - Algumas ❍ foram adicionadas no sistema X em equilíbrio.
Alteração 2 - A temperatura do sistema X em equilíbrio foi aumentada.
Alteração 3 - A pressão do sistema X em equilíbrio foi aumentada.
A seguir estão representados os sistemas Y, Z, W, T e J, todos em equilíbrio químico, que podem representar as alterações ocorridas.
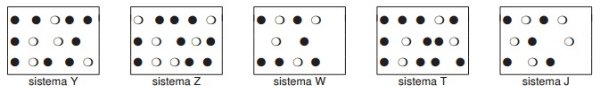
Com base no enunciado e nos conhecimentos sobre equilíbrio químico, considere as afirmativas.
I. O sistema Z é aquele que melhor representa a nova posição de equilíbrio após a alteração 1 no sistema X.
II. O sistema J é aquele que melhor representa a nova posição de equilíbrio após a alteração 2 no sistema X.
III. O sistema W é aquele que melhor representa a nova posição de equilíbrio após a alteração 3 no sistema X.
IV. Os sistemas Y e T são aqueles que melhor representam as novas posições de equilíbrio após as alterações 2 e 3, respectivamente no sistema X
alguém por favor pode me explicar detalhadamente o pq a III esta correta?
Algumas alterações foram realizadas, separada e individualmente, no sistema X.
Alteração 1 - Algumas ❍ foram adicionadas no sistema X em equilíbrio.
Alteração 2 - A temperatura do sistema X em equilíbrio foi aumentada.
Alteração 3 - A pressão do sistema X em equilíbrio foi aumentada.
A seguir estão representados os sistemas Y, Z, W, T e J, todos em equilíbrio químico, que podem representar as alterações ocorridas.
Com base no enunciado e nos conhecimentos sobre equilíbrio químico, considere as afirmativas.
I. O sistema Z é aquele que melhor representa a nova posição de equilíbrio após a alteração 1 no sistema X.
II. O sistema J é aquele que melhor representa a nova posição de equilíbrio após a alteração 2 no sistema X.
III. O sistema W é aquele que melhor representa a nova posição de equilíbrio após a alteração 3 no sistema X.
IV. Os sistemas Y e T são aqueles que melhor representam as novas posições de equilíbrio após as alterações 2 e 3, respectivamente no sistema X
alguém por favor pode me explicar detalhadamente o pq a III esta correta?
kayron winkell- Recebeu o sabre de luz

- Mensagens : 170
Data de inscrição : 12/10/2016
Idade : 26
Localização : juazeiro do norte
 Re: equilíbrio químico
Re: equilíbrio químico
Saudações!
Quando se aumenta a pressão do sistema, há um deslocamento para o sentido com o menor número de mols (menor volume).
Acontece que na reação apresentada, há um mol nos reagentes e um mol nos produtos.
Portanto, aumentar a pressão não mudará nada.
O único em que as quantidades da bolinha preta e da bolinha branca são iguais ao do sistema X é o sistema W.
Espero ter ajudado!
Quando se aumenta a pressão do sistema, há um deslocamento para o sentido com o menor número de mols (menor volume).
Acontece que na reação apresentada, há um mol nos reagentes e um mol nos produtos.
Portanto, aumentar a pressão não mudará nada.
O único em que as quantidades da bolinha preta e da bolinha branca são iguais ao do sistema X é o sistema W.
Espero ter ajudado!

muuhmuuhzao- Jedi

- Mensagens : 216
Data de inscrição : 01/04/2021
kayron winkell gosta desta mensagem
 Re: equilíbrio químico
Re: equilíbrio químico
eu levei em consideração o fato de termos 4 moléculas ❍ e 6 de ● , então achei que o resultado fosse diferente , pois nao seria a mesma quantidademuuhmuuhzao escreveu:Saudações!
Quando se aumenta a pressão do sistema, há um deslocamento para o sentido com o menor número de mols (menor volume).
Acontece que na reação apresentada, há um mol nos reagentes e um mol nos produtos.
Portanto, aumentar a pressão não mudará nada.
O único em que as quantidades da bolinha preta e da bolinha branca são iguais ao do sistema X é o sistema W.
Espero ter ajudado
kayron winkell- Recebeu o sabre de luz

- Mensagens : 170
Data de inscrição : 12/10/2016
Idade : 26
Localização : juazeiro do norte
 Re: equilíbrio químico
Re: equilíbrio químico
Em alguns casos de fato a reação dada não está balanceada (já vi isso em questão da UNICAMP), mas nesses casos eles terão que dar algum indicativo de que o balanceamento não é o que indicaram. Isso pode ser feito mostrando o gráfico da reação, como foi feito na questão da UNICAMP, assim seria possível saber o quanto teve que reagir da substância X para formar a Y.
Mas nessa questão não dá para fazer isso, pois não indicaram. O fato de ter 4 de uma e 6 da outra não quer dizer que a relação estequiométrica não é de 1:1. Por exemplo, podia ter no início 10 mols da clara, reagiram 6 mols e formaram 6 mols da bola escura (proporção de 1 para 1). Sobrariam 4 da clara e 6 da escura no equilíbrio.
Mas nessa questão não dá para fazer isso, pois não indicaram. O fato de ter 4 de uma e 6 da outra não quer dizer que a relação estequiométrica não é de 1:1. Por exemplo, podia ter no início 10 mols da clara, reagiram 6 mols e formaram 6 mols da bola escura (proporção de 1 para 1). Sobrariam 4 da clara e 6 da escura no equilíbrio.

muuhmuuhzao- Jedi

- Mensagens : 216
Data de inscrição : 01/04/2021
 Re: equilíbrio químico
Re: equilíbrio químico
nossa! valeu ,dei bobeira nessamuuhmuuhzao escreveu:Em alguns casos de fato a reação dada não está balanceada (já vi isso em questão da UNICAMP), mas nesses casos eles terão que dar algum indicativo de que o balanceamento não é o que indicaram. Isso pode ser feito mostrando o gráfico da reação, como foi feito na questão da UNICAMP, assim seria possível saber o quanto teve que reagir da substância X para formar a Y.
Mas nessa questão não dá para fazer isso, pois não indicaram. O fato de ter 4 de uma e 6 da outra não quer dizer que a relação estequiométrica não é de 1:1. Por exemplo, podia ter no início 10 mols da clara, reagiram 6 mols e formaram 6 mols da bola escura (proporção de 1 para 1). Sobrariam 4 da clara e 6 da escura no equilíbrio.
kayron winkell- Recebeu o sabre de luz

- Mensagens : 170
Data de inscrição : 12/10/2016
Idade : 26
Localização : juazeiro do norte
muuhmuuhzao gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico - grau de equilíbrio
» Equilíbrio químico
» Equilíbrio químico
» Equilíbrio Químico ....
» Equilíbrio Químico
» Equilíbrio químico
» Equilíbrio químico
» Equilíbrio Químico ....
» Equilíbrio Químico
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













