Precipitado na presença de íons. Ajuda?
2 participantes
Página 1 de 1
 Precipitado na presença de íons. Ajuda?
Precipitado na presença de íons. Ajuda?
(PUC-C) Os ânions presentes nas soluções aquosas NaCl, KBr e RbI formam precipitados em presença de íons:
a)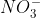
B)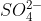
c)
d) Li+
e)Ag+
por favor tentem me explicar qual forma o precipitado e quais não formam e porque. Estou com dificuldades em entender isso.
a)
B)
c)
d) Li+
e)Ag+
por favor tentem me explicar qual forma o precipitado e quais não formam e porque. Estou com dificuldades em entender isso.

puiff- Mestre Jedi

- Mensagens : 547
Data de inscrição : 17/02/2012
Idade : 29
Localização : Jacareí - SP
 Re: Precipitado na presença de íons. Ajuda?
Re: Precipitado na presença de íons. Ajuda?
Aí é estudar...
Não tem jeito.
Os ELEMENTOS são como todos os elementos...
Alguns parecidos formam uma "tchurma", uma "família", "grupo", como os Metais Alcalinos: Li, Na, K, Rb, Cs, Fr.
Cada um é um indivíduo diferente do seu parceiro de turma, mas compartilham algo em comum: adoram dar seu elétron da última camada e sempre se transformam num íon positivo (cátion) com carga 1+ !
Geralmente são muito solúveis em água quase sempre se dissociando completamente (100%) de seus ânions (íons negativos):
NaCl ----aq-----> Na¹+ + Cl ¹-
O mesmo não acontece com a Prata, Ag, e seu cátion, Ag¹+.
Ela se gruda com o ânion do cloro, o cloreto (Cl¹-) e os de sua "tchurma", os Halogêneos, F, Br, I e At , e não é fácil separá-los !!!
Assim, não se dissociam na água, ficando juntinhos e indo parar no fundo da solução, agora mistura heterogênea.
São uma poucas "regras", rapidinho você as aprende ! :study: :geek:
Não tem jeito.
Os ELEMENTOS são como todos os elementos...
Alguns parecidos formam uma "tchurma", uma "família", "grupo", como os Metais Alcalinos: Li, Na, K, Rb, Cs, Fr.
Cada um é um indivíduo diferente do seu parceiro de turma, mas compartilham algo em comum: adoram dar seu elétron da última camada e sempre se transformam num íon positivo (cátion) com carga 1+ !
Geralmente são muito solúveis em água quase sempre se dissociando completamente (100%) de seus ânions (íons negativos):
NaCl ----aq-----> Na¹+ + Cl ¹-
O mesmo não acontece com a Prata, Ag, e seu cátion, Ag¹+.
Ela se gruda com o ânion do cloro, o cloreto (Cl¹-) e os de sua "tchurma", os Halogêneos, F, Br, I e At , e não é fácil separá-los !!!
Assim, não se dissociam na água, ficando juntinhos e indo parar no fundo da solução, agora mistura heterogênea.
São uma poucas "regras", rapidinho você as aprende ! :study: :geek:
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
 Re: Precipitado na presença de íons. Ajuda?
Re: Precipitado na presença de íons. Ajuda?
Bom, algums coisas eu sei, só não entendi por que no caso é a prata que forma o precipitado e não o lítio.

puiff- Mestre Jedi

- Mensagens : 547
Data de inscrição : 17/02/2012
Idade : 29
Localização : Jacareí - SP
 Re: Precipitado na presença de íons. Ajuda?
Re: Precipitado na presença de íons. Ajuda?
É só reler o que escrevi :face:
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
 Re: Precipitado na presença de íons. Ajuda?
Re: Precipitado na presença de íons. Ajuda?
Bom, reli e entendi, mas ainda me falta praticar muito, obrigada pela ajuda. ^^

puiff- Mestre Jedi

- Mensagens : 547
Data de inscrição : 17/02/2012
Idade : 29
Localização : Jacareí - SP
 Re: Precipitado na presença de íons. Ajuda?
Re: Precipitado na presença de íons. Ajuda?
Estudar primeiro :study: ! :study:
Praticar muito :bounce:, depois ! :bounce:
Praticar muito :bounce:, depois ! :bounce:
rihan- Estrela Dourada

- Mensagens : 5049
Data de inscrição : 22/08/2011
Idade : 69
Localização : Rio de Janeiro, RJ, Itabuna-Ilhéus, BA, Brasil
 Tópicos semelhantes
Tópicos semelhantes» % da presença do elemento
» formação precipitado
» Precipitado em Solução
» Tampão e Precipitado
» Formação de precipitado
» formação precipitado
» Precipitado em Solução
» Tampão e Precipitado
» Formação de precipitado
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












