Tabela Periódica
2 participantes
Página 1 de 1
 Tabela Periódica
Tabela Periódica
As representações de átomos, moléculas, íons, etc. são comumente feitas utilizando-se esferas de tamanhos diferentes. O tamanho destas esferas tenta, fora de escala, representar a diferença entre as dimensões dos diferentes átomos. O retículo cristalino formado pelos íons Na+ (Z = 11) e Cl- (Z = 17) pode ser representado da seguinte forma:
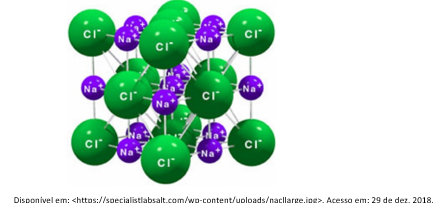
Caso fosse necessário representar a estrutura do composto formado pelos íons isoeletrônicos K+ (Z = 19) e Cl-, a dimensão do íon K+ seria

Caso fosse necessário representar a estrutura do composto formado pelos íons isoeletrônicos K+ (Z = 19) e Cl-, a dimensão do íon K+ seria
A
maior que a do íon Cl-, uma vez que sua carga nuclear é maior.
B
maior que a do íon Cl-, uma vez que sua carga nuclear é menor.
C
menor que a do íon Cl-, uma vez que sua carga nuclear é maior.
D
menor que a do íon Cl-, uma vez que sua carga nuclear é menor.
E
igual à do íon Cl-, uma vez que suas cargas nucleares são iguais.
Última edição por Anya Engel em Qui 14 Abr 2022, 11:35, editado 1 vez(es)

Anya Engel- Recebeu o sabre de luz

- Mensagens : 139
Data de inscrição : 14/09/2021
 Re: Tabela Periódica
Re: Tabela Periódica
Como ambos vão ter a mesma quantidade de elétrons e a mesma configuração dos orbitais, aquele que tiver a maior quantidade de protons terá uma maior atração eletrosfera - núcleo, o que vai diminuir o raio atômico.
Ou seja, o K+, por possuir mais protons que o Cl-, vai possuir um raio menor, pois vai atrair mais fortemente o ultimo elétron
K(19) 1s2 2s2 2p6 3s2 3p6 4s1 --> K+ 1s2 2s2 2p6 3s2 3p6
Cl(17) 1s2 2s2 2p6 3s2 3p5 --> Cl- 1s2 2s2 2p6 3s2 3p6
Letra C).
Ou seja, o K+, por possuir mais protons que o Cl-, vai possuir um raio menor, pois vai atrair mais fortemente o ultimo elétron
K(19) 1s2 2s2 2p6 3s2 3p6 4s1 --> K+ 1s2 2s2 2p6 3s2 3p6
Cl(17) 1s2 2s2 2p6 3s2 3p5 --> Cl- 1s2 2s2 2p6 3s2 3p6
Letra C).

gusborgs- Mestre Jedi

- Mensagens : 715
Data de inscrição : 27/08/2021
 Re: Tabela Periódica
Re: Tabela Periódica
Obrigada por reponder a questão

Anya Engel- Recebeu o sabre de luz

- Mensagens : 139
Data de inscrição : 14/09/2021
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos













