ufrgs 2016 química Q48 eletroquímica
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 ufrgs 2016 química Q48 eletroquímica
ufrgs 2016 química Q48 eletroquímica
O quadro abaixo relaciona algumas semirreações e seus respectivos potenciais padrão de redução, em solução aquosa.
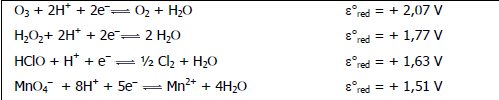
A partir desses dados, é correto afirmar que
(A) uma solução aquosa de hipoclorito poderá oxidar os íons Mn2+.
(B) uma solução aquosa de H2O2 é um forte agente redutor.
(C) o ozônio tem uma forte tendência a ceder elétrons em solução aquosa.
(D) a adição de H2O2 a uma solução aquosa, contendo oxigênio dissolvido, promove a formação de ozônio gasoso.
(E) o permanganato, entre as substâncias relacionadas no quadro, é o mais poderoso agente oxidante.
Poderiam resolver? Fiz assim e fiquei com essas dúvidas:
A) correta, pois a semirreação de redução do MnO4- tem potencial de redução menor, o que faria com que ele fosse o oxidado
B) é um forte agente oxidante
C) tem uma forte tendência a receber elétrons
D) ??
E) falso, o agente oxidante menos poderoso.
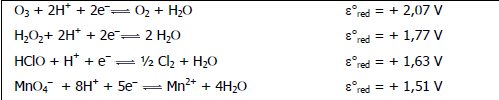
A partir desses dados, é correto afirmar que
(A) uma solução aquosa de hipoclorito poderá oxidar os íons Mn2+.
(B) uma solução aquosa de H2O2 é um forte agente redutor.
(C) o ozônio tem uma forte tendência a ceder elétrons em solução aquosa.
(D) a adição de H2O2 a uma solução aquosa, contendo oxigênio dissolvido, promove a formação de ozônio gasoso.
(E) o permanganato, entre as substâncias relacionadas no quadro, é o mais poderoso agente oxidante.
Poderiam resolver? Fiz assim e fiquei com essas dúvidas:
A) correta, pois a semirreação de redução do MnO4- tem potencial de redução menor, o que faria com que ele fosse o oxidado
B) é um forte agente oxidante
C) tem uma forte tendência a receber elétrons
D) ??
E) falso, o agente oxidante menos poderoso.
Última edição por folettinhomed em Qui 19 Set 2019, 17:57, editado 1 vez(es)

folettinhomed- Mestre Jedi

- Mensagens : 988
Data de inscrição : 23/02/2019
Idade : 24
Localização : Santa Cruz do Sul, RS, Brasil
 Re: ufrgs 2016 química Q48 eletroquímica
Re: ufrgs 2016 química Q48 eletroquímica
EXPLICAÇÃO ALTERNATIVA D: O que eu entendi é que devem ser comparados os potenciais... Numa reação H202 e O3 (já com presença de produtos na solução), o ozônio tem um maior poder de redução, ou seja, espontaneamente, irá ocorrer oxidação do H2O2 e o O3 manterá o sentido direto de sua reação (redução) formando oxigênio e água.
brunerguilherme- Iniciante
- Mensagens : 37
Data de inscrição : 18/09/2019
Idade : 27
Localização : Leme/SP
 Re: ufrgs 2016 química Q48 eletroquímica
Re: ufrgs 2016 química Q48 eletroquímica
Então a reação ficaria assim?
O3 + 2 H+ + 2e -----> O2 + H2O
2 H2O ---> H2O2 + 2 H+ + 2e
Promovendo a formação de O2 gasoso?
O3 + 2 H+ + 2e -----> O2 + H2O
2 H2O ---> H2O2 + 2 H+ + 2e
Promovendo a formação de O2 gasoso?

folettinhomed- Mestre Jedi

- Mensagens : 988
Data de inscrição : 23/02/2019
Idade : 24
Localização : Santa Cruz do Sul, RS, Brasil
 Re: ufrgs 2016 química Q48 eletroquímica
Re: ufrgs 2016 química Q48 eletroquímica
Pelo meu entender, sim. Mas realmente ficou confusa essa diretriz da alternativa D porque é necessário subentender que o ozônio já está presente na água... Já que sabemos que redução/oxidação da água e do oxigênio não resultam nesses compostos (H2O2 e O3).
brunerguilherme- Iniciante
- Mensagens : 37
Data de inscrição : 18/09/2019
Idade : 27
Localização : Leme/SP
 Re: ufrgs 2016 química Q48 eletroquímica
Re: ufrgs 2016 química Q48 eletroquímica
Qual o erro em imaginar O2 e H2O2, como reagentes, entao pegando suas semi-reacoes?
Meu raciocinio foi
O2 + H2O ----->O3 + 2 H+ + 2e
(inverti essa, então inverti o sinal da ddp) : -2,07
e
H2O2 + 2 H+ + 2e ---> 2 H2O +1,77
Dando a global:
O2 +H2O2 ---> O3 + H2O -0,3
Dando o O3...
Qual o erro disso? Seria pq quando ele diz "oxigênio dissolvido", esse dissolvido é pq a reação já ocorreu como afirmou o brunerguilherme e portanto "Oxigenio dissolvido" é sempre um produto?
Meu raciocinio foi
O2 + H2O ----->O3 + 2 H+ + 2e
(inverti essa, então inverti o sinal da ddp) : -2,07
e
H2O2 + 2 H+ + 2e ---> 2 H2O +1,77
Dando a global:
O2 +H2O2 ---> O3 + H2O -0,3
Dando o O3...
Qual o erro disso? Seria pq quando ele diz "oxigênio dissolvido", esse dissolvido é pq a reação já ocorreu como afirmou o brunerguilherme e portanto "Oxigenio dissolvido" é sempre um produto?

Raquel Valadão- Mestre Jedi

- Mensagens : 523
Data de inscrição : 04/04/2017
Localização : Bahia
 Re: ufrgs 2016 química Q48 eletroquímica
Re: ufrgs 2016 química Q48 eletroquímica
Acho que seria pq estaria em contato com H2O, como você descreveu na reação. Mas acho que você não deveria inverter essa equação, e sim a outra, por análise dos potenciais

folettinhomed- Mestre Jedi

- Mensagens : 988
Data de inscrição : 23/02/2019
Idade : 24
Localização : Santa Cruz do Sul, RS, Brasil
 Tópicos semelhantes
Tópicos semelhantes» ufrgs 2016 química Q47 KC
» ufrgs 2016 química Q32
» ufrgs 2016 química Q40
» ufrgs 2016 química Q43
» ufrgs 2016 química Q46
» ufrgs 2016 química Q32
» ufrgs 2016 química Q40
» ufrgs 2016 química Q43
» ufrgs 2016 química Q46
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












