Ponto de fusão e energia de ionização
2 participantes
Página 1 de 1
 Ponto de fusão e energia de ionização
Ponto de fusão e energia de ionização
Os dados X e Y que faltam no quadro são:

A) X= 770; Y= 141
B) X= 861; Y= 1430
C) X= 1550; Y= 141
D) X= 770; Y= 1430
A) X= 770; Y= 141
B) X= 861; Y= 1430
C) X= 1550; Y= 141
D) X= 770; Y= 1430

Rennan Santos- Padawan

- Mensagens : 52
Data de inscrição : 14/01/2023
Idade : 17
Localização : Itaguai - Rio de Janeiro - Brasil
 Re: Ponto de fusão e energia de ionização
Re: Ponto de fusão e energia de ionização
Para descobrir o ponto de fusão do Estrôncio é preciso lembrar que o ponto de fusão dos elementos da parte esquerda da tabela periódica crescem de baixo para cima em cada grupo(ou família), assim o ponto de fusão do estrôncio será maior que o P.F. do Bário e menor que o P.F. do Cálcio, e por análise das alternativas podemos perceber que o ponto de fusão do Estrôncio será 770ºC.
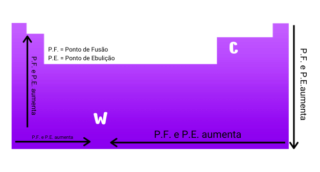
Agora para a análise da primeira energia de ionização do Cálcio deve-se lembrar que a energia de ionização cresce de baixo para cima em cada grupo e da esquerda para a direita em cada período, o que nos leva a conclusão de que a primeira energia de ionização do cálcio é maior que a do estrôncio e do que a do bário, o que de fato é satisfeito em todas as alternativas, portanto deve-se considerar que, apesar da energia de ionização do cálcio ser maio que a do estrôncio e a do bário, ele ainda é um metal alcalino que é o grupo com menor energia de ionização da tabela periódica o que implica a impossibilidade de ocorrer um salto tão grande da energia de ionização como ocorreria se a energia de ionização do cálcio fosse 1430 Kcal/mol portanto a energia de ionização do cálcio será 141 Kcal/ mol, como parâmetro de comparação a primeira energia de ionização do hélio, a maior das primeiras energias de ionização, é aproximadamente 567 Kcal/mol.

Agora para a análise da primeira energia de ionização do Cálcio deve-se lembrar que a energia de ionização cresce de baixo para cima em cada grupo e da esquerda para a direita em cada período, o que nos leva a conclusão de que a primeira energia de ionização do cálcio é maior que a do estrôncio e do que a do bário, o que de fato é satisfeito em todas as alternativas, portanto deve-se considerar que, apesar da energia de ionização do cálcio ser maio que a do estrôncio e a do bário, ele ainda é um metal alcalino que é o grupo com menor energia de ionização da tabela periódica o que implica a impossibilidade de ocorrer um salto tão grande da energia de ionização como ocorreria se a energia de ionização do cálcio fosse 1430 Kcal/mol portanto a energia de ionização do cálcio será 141 Kcal/ mol, como parâmetro de comparação a primeira energia de ionização do hélio, a maior das primeiras energias de ionização, é aproximadamente 567 Kcal/mol.

TatsuoPlays43- Iniciante
- Mensagens : 13
Data de inscrição : 16/01/2022
Idade : 18
Localização : Brasília
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













