Máquinas Térmicas
3 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Máquinas Térmicas
Máquinas Térmicas
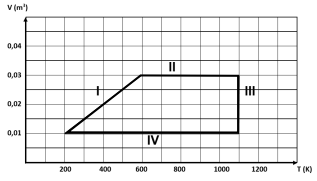
Um gás ideal passa pelas transformações I, II, III e IV, voltando ao estado inicial de volume 0,01 m3 e temperatura de 200 K, como representado no diagrama volume X temperatura a seguir. Imagem associada para resolução da questão.
De acordo com o diagrama, é correto afirmar que durante o processo
Alternativas
A)I o gás passa por uma transformação adiabática.
B)II é realizado trabalho sobre o gás.
C)III o gás perde calor para a vizinhança.
D)IV a energia interna do gás aumenta.
Alguém poderia explicar como chegar nessa resposta?
Qual o motivo de não ser a alternativa D? A questão pergunta o que ocorre durante o processo. No gráfico dá para ver que a temperatura do gás aumenta no percurso ll. Como a energia é proporcional a temperatura, então a energia também aumenta.
De acordo com o diagrama, é correto afirmar que durante o processo

Alternativas
A)I o gás passa por uma transformação adiabática.
B)II é realizado trabalho sobre o gás.
C)III o gás perde calor para a vizinhança.
D)IV a energia interna do gás aumenta.
- Spoiler:
- Resposta: C
Alguém poderia explicar como chegar nessa resposta?
Qual o motivo de não ser a alternativa D? A questão pergunta o que ocorre durante o processo. No gráfico dá para ver que a temperatura do gás aumenta no percurso ll. Como a energia é proporcional a temperatura, então a energia também aumenta.
samuelbelembr@gmail.com- Jedi

- Mensagens : 205
Data de inscrição : 04/10/2021
 Re: Máquinas Térmicas
Re: Máquinas Térmicas
E aí, Samuel.
Primeiro, observe que os processos se dão no caminho horário: I -> II -> III -> IV
Chegamos à resposta C ao analisarmos o processo III: o volume diminui (compressão) e a temperatura permanece constante. Isso acontece quando toda a energia transferida pelo trabalho realizado sobre o gás é transferida para a vizinhança em forma de calor — se não fosse o caso, a temperatura do gás deveria aumentar, já que haveria um aumento de sua energia interna.
O que invalida a alternativa D é o fato de que, durante o processo IV, a temperatura diminui. Como você disse, há proporcionalidade entre temperatura e energia. Sendo assim, uma menor temperatura implica menor energia.
Primeiro, observe que os processos se dão no caminho horário: I -> II -> III -> IV
Chegamos à resposta C ao analisarmos o processo III: o volume diminui (compressão) e a temperatura permanece constante. Isso acontece quando toda a energia transferida pelo trabalho realizado sobre o gás é transferida para a vizinhança em forma de calor — se não fosse o caso, a temperatura do gás deveria aumentar, já que haveria um aumento de sua energia interna.
O que invalida a alternativa D é o fato de que, durante o processo IV, a temperatura diminui. Como você disse, há proporcionalidade entre temperatura e energia. Sendo assim, uma menor temperatura implica menor energia.

antoniolcn- Padawan

- Mensagens : 61
Data de inscrição : 08/11/2020
Idade : 22
 Re: Máquinas Térmicas
Re: Máquinas Térmicas
Apenas completando a resolução do colega Antônio.
Em todos os ciclos termodinâmicos a variação de energia interna é nula, haja vista que ao fim do ciclo o meio retorna às temperaturas e pressões iniciais.
Em todos os ciclos termodinâmicos a variação de energia interna é nula, haja vista que ao fim do ciclo o meio retorna às temperaturas e pressões iniciais.

Jvictors021- Estrela Dourada

- Mensagens : 1116
Data de inscrição : 02/07/2021
Idade : 20
Localização : Passa Quatro - MG
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













